乳腺癌细胞是如何转移的
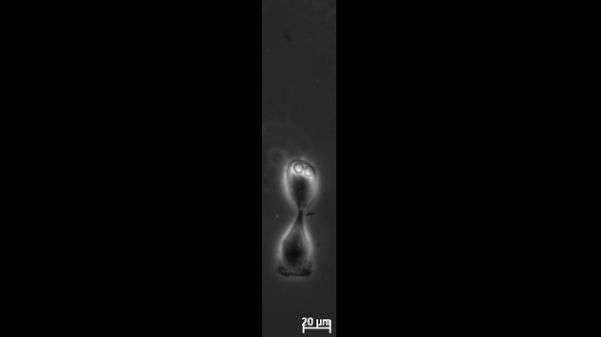
将癌细胞从身体的一部分蔓延到另一部分,一种称为转移的过程,是癌症患者中死亡的主要原因。4月26日公布的一项研究生物物理学杂志现在揭示了为什么某些癌细胞比其他癌细胞可能更加转移。结果表明,乳腺癌细胞通过围绕原始肿瘤滑动其逃逸路线的其他电池滑动到身体的其他部位。
“我们展示了一种定量的标尺来测量细胞滑动的能力,”美国东北大学的资深研究作者Anand Asthagiri说。“通过对这种细胞行为进行数字分析,我们不仅可以辨别哪些路径调节滑动,还可以辨别滑动的大小。”这为找到最有力的滑动行为驱动因素和遏制这种侵入性行为的策略打开了大门。”
侵入身体中的其他组织,癌细胞沿着胶原蛋白纤维迁移,作为走出原发肿瘤的途径。但是这些纤维非常狭窄,微环境中挤满了其他细胞,所以转移性癌细胞是如何克服障碍并成功地在这个空间有限的环境中生存的还不清楚。
“请记住,每个细胞都是10-15微米宽,并寻找一种方法来挥舞邻居,也10-15微米宽。他们在只有5μm宽的轨道上完成所有这一切,”asthagiri说。“他们如何挤压,延伸和包装是非常显着的,并且是一个令人着迷的生物物理问题。我们非常有兴趣整理机制和调节细胞如何完成这一点,以及为什么癌细胞特别擅长。”
为了回答这个问题,Asthagiri和他的团队在玻璃表面贴上了微图案的纤维连接蛋白线,然后使用延时显微镜来研究沉积在粘附纤维上的细胞对之间的碰撞。在仅6 μm或9 μm宽的微模式模拟肿瘤环境条件下,99%的正常乳腺细胞在与另一个细胞物理接触时停止并逆转方向。相比之下,大约一半的转移乳腺癌细胞对碰撞的反应是滑过另一个细胞,保持它们沿着蛋白质轨道的迁移路径。
然而,当研究人员将微图宽度增加到33μm或减少将细胞结合在一起的粘膜蛋白的粘膜蛋白减少时,正常的乳房细胞更可能滑过其他细胞。同时,e-cadherin水平的增加减少了转移的滑动行为乳腺癌细胞。
额外的实验表明,PARD3,ERBB2和TGFβ-蛋白涉及转移配合以调节细胞滑动行为。在一起,调查结果证明了细胞滑动在支持转移中的关键作用,以及允许这种情况发生的分子途径。
在未来的研究中,测试这些发现是否能延伸到更复杂、更现实的模拟肿瘤环境的条件将是很重要的,在这种环境中,不同类型的细胞经常相互碰撞。就他们自己而言,研究人员计划进一步探索潜在的分子机制,并测试他们开发的系统是否可以作为一个筛选平台,以找到抑制细胞滑动的分子目标。
“因为我们的结果提供了一种尺寸衡量遗传扰动能够滑动的程度的统治者,它提供了一种排序顺序分子途径的方法,并鉴定对具有协同效应的基因的组合滑动潜力,”Asthagiri说。“滑动,以及我们认为更广泛的侵入性,是一种逐步积累的属性,随着每个促进癌症的事件可测量地改变侵入性的程度。有了尺子,我们就可以量化细胞的转化程度,以及一种疗法相对于另一种疗法的有效性。”
进一步探索










用户评论