癌症研究人员在卵巢癌肿瘤生长上发布新纸张

涉及Notre Dame大学汉普尔癌研究所(HCRI)涉及卵巢癌研究的两篇论文,其中一项新的研究和其他一篇审查条款被公布为各自期刊的封面故事。
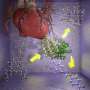
HCRI主任m·莎伦·斯塔克(M. Sharon Stack)、安妮·f·邓恩(Anne F. Dunne)和伊丽莎白·赖利(Elizabeth Riley),以及博士后研究员杨静(Jing Yang)和尤利娅·克里门科(Yuliya Klymenko)等人一直在研究卵巢癌细胞在腹腔内扩散的独特原因。在腹腔内,脱落的卵巢癌细胞结合在一起,形成一种叫做聚集体的致命结构。这些聚集体漂浮在腔内,直到最终粘附并穿透更多的组织。这种转移模式,再加上模糊的症状导致诊断延迟,使卵巢癌成为最致命的癌症之一。
在他们的文章中发表生物化学杂志(JBC),杨,堆和同事研究了一种膜蛋白酶,称为MT1-MMP,这是一种开始结缔组织蛋白击穿的酶。MT1-MMP通常在正常的卵巢组织中甚至在良性卵巢肿瘤中未检测到。
MT1-MMP包括短细胞质尾部或20个氨基酸链,其调节细胞表面上的活性。尾部包含三个潜在的地方,其中调节蛋白质,称为磷酸化位点。杨的和堆栈的研究表明,磷酸化可能在调节卵巢癌细胞从“浮动”相到“粘贴”相中的转变起作用腹腔。
“MT1是细胞表面的一种分子剪子,它剪掉这些蛋白质,就像我们剪掉树根,为其他植物腾出更多空间一样,”斯塔克说。”卵巢癌细胞,这使得它们更好地粘得它们茁壮成长。“并变得贴满意味着更多的转移成功 - 有效地将癌症传播到身体的新区域。
Stack说,这一发现很重要,因为了解不同的磷酸化位点是如何起作用的,可能会导致发现靶向和抑制这一过程的药物。
审查文件发表在癌症8月份是32页概述,由Klymenko,Stack和Oleg Kim举办了应用的计算数学和统计数据部的兼职教授,总结了当前研究卵巢癌转移和化学性。本文还概述了有助于理解这些过程的计算模型。
斯塔克说,她和她的团队今年夏天很荣幸能在两家杂志的封面上发表他们的研究成果——这是她的研究第三次出现在封面上,也是第一次在一个月内有两篇文章出现在封面上。另一项评估胎次(女性分娩的次数)对转移的影响的研究已经被接受癌症字母。一项关于衰老对转移的研究已提交并正在审查中。
“我们在哈珀大学所做的研究让我们更接近于回答卵巢特有的问题癌症“堆栈说。”这最终会为越来越多的治疗方案铺平道路,目的是增加女性的生存率卵巢癌。"
进一步探索
Yuliya Klymenko等人。卵巢癌中上皮细胞表型可塑性的复杂决定因素癌症(2017)。DOI:10.3390 /癌症9080104








用户评论