研究显示新型抗kras药物有望治疗胰腺癌
来自宾夕法尼亚大学医学院艾布拉姆森癌症中心的研究人员表示,在近30%的人类肿瘤中发现的一种小分子抑制剂,可以攻击难以靶向的致癌基因突变KRAS,在胰腺癌临床前模型中成功缩小肿瘤或阻止癌症生长,这表明该药物是临床试验的强有力候选药物。这项研究今天发表在癌症的发现.
“这项研究的结果与我们之前在研究中看到的任何结果形成了鲜明的对比胰腺癌共同通讯的资深作者本·斯坦格博士说,他是宾夕法尼亚大学佩雷尔曼医学院癌症研究的汉娜·怀斯教授,也是宾夕法尼亚胰腺癌研究中心的主任。“即使在临床前研究模型中也是如此癌症类型在美国,过去十年中测试的大多数药物——包括新的免疫疗法——影响有限。”
胰腺癌患者有一个整体预后不良5年生存率为11%,治疗方案有限。近90%的胰腺癌是由KRAS基因突变引起的,KRAS基因是癌症类型中最常见的致癌基因。KRAS的第一个靶向治疗去年被批准用于非小细胞肺癌与KRAS G12C突变有关,但只有2%的胰腺癌表达这种类型的突变。大约36%的KRAS突变胰腺癌是KRAS g12d突变。
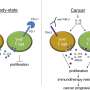
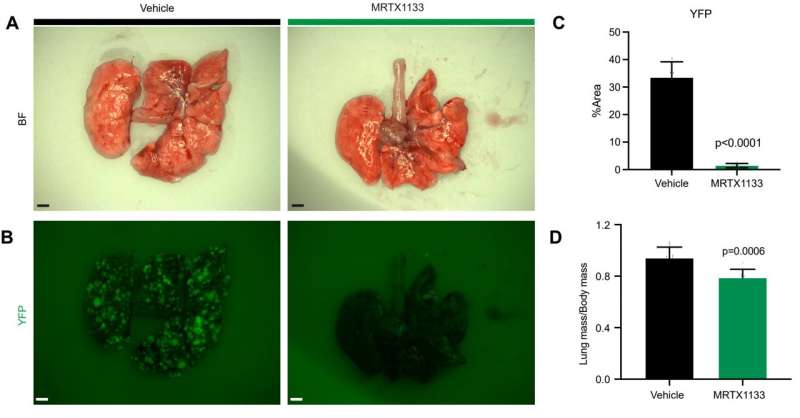
这项研究中使用的小分子抑制剂MRTX1133(由Mirati Therapeutics开发)专门针对KRAS G12D,正如该公司上个月首次报道的那样自然医学.宾夕法尼亚大学的研究现在表明kras抑制剂不仅直接靶向癌症细胞但也出人意料地与免疫系统合作,对治疗产生持久的反应,这很重要,因为癌症最终会找到逃避大多数靶向治疗的方法。
斯坦格说:“我们从KRAS G12C研究和其他靶向治疗研究中得知,耐药性将会发生。”“甚至在我们到达之前临床试验在美国,我们正在考虑如何联合用药,这样肿瘤就不会复发。我们的研究结果为免疫疗法与KRAS G12D抑制剂的合作提供了证据。”
研究人员能够评估MRTX1133对免疫系统的影响,因为研究中使用的模型类型允许肿瘤在植入健康小鼠后自发进化,从而有可能辨别药物对周围肿瘤微环境(TME)的影响。
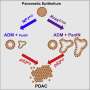
免疫能力KPC模型是由宾夕法尼亚大学医学院近20年前开发的,是全球用于评估胰腺导管腺癌(PDAC)潜在疗法的金标准。众所周知,PDAC具有特别密集的TME,这有助于抵抗治疗。
研究小组发现,该药物促进了TME中T细胞的增加,从而提高了对MRTX1133的反应深度和持续时间。研究中观察到的所有完全缓解都伴随着T细胞介导的抗肿瘤免疫。在没有T细胞的小鼠中,MRTX1133的作用是短暂的,肿瘤生长得更快。这些结果表明,MRTX1133可以与免疫治疗联合使用,以改善对治疗的长期反应,并防止癌症复发。
“经过多年的工作,为胰腺癌患者寻找急需的新方法,令人兴奋的是,一种新的药物即将出现,”共同通讯作者罗伯特·冯德海德博士说,他是艾布拉姆森癌症中心主任,佩雷尔曼医学院的约翰·h·格里克·艾布拉姆森癌症中心教授,他的实验室成员与斯坦格实验室的人在这项研究中进行了集中合作。
“我们乐观地认为,KRAS G12D抑制剂将很快进入临床试验。KRAS投降了,现在我们知道免疫系统我能看到。”
Jill Hallin等人,一种有效的选择性非共价KRASG12D抑制剂的抗肿瘤疗效,自然医学(2022)。DOI: 10.1038 / s41591 - 022 - 02007 - 7