肌肉转化为脂肪:多能干细胞的错误命运驱动LGMD2B

2019年6月3日在线发布的儿童国家教师领导的研究自然通讯研究表明,2型肢体带肌萎缩症(LGMD2B)症状的突然出现是促进健康肌肉修复的不同细胞类型之间交流受损的结果。特别有趣的是纤维/脂肪生成前体(FAPs),这种细胞通常通过清除碎片和促进肌肉细胞与新肌纤维的融合,在损伤后的肌肉再生中发挥有益作用。
LGMD2B是由Dysf基因的突变造成的,损害Dysferlin的功能,这是修复受伤的蛋白质肌肉纤维。患者直到成年后才会出现攀爬或跑步困难等症状。这种迟发性疾病一直困扰着研究人员,因为dysferlin缺失的细胞后果从出生开始就存在,并持续发展,但直到患者晚年才会产生影响。
该研究发现,在不存在脓剂藻的情况下,肌肉逐渐增加蛋白质膜蛋白A2的表达,例如Dysferlin,促进受伤肌纤维的修复。然而,增加膜蛋白A2积聚在肌纤维外,并驱动肌肉内的Faps的增加,并鼓励这些Faps分化为脂肪细胞,形成脂肪沉积物。使用现成的药物抑制粘性药物的脂肪替代粘性药物肌肉粘连或阻断腹膜蛋白A2或阻塞FAP的adipyyte命运。
“我们提出了一个前馈回路,在这个回路中,反复的肌纤维损伤会引发慢性炎症,随着时间的推移,这会创造一种环境,促进FAPs积累并分化为脂肪。Jyoti K. Jaiswal说。Jyoti K. Jaiswal是国家儿童基金会遗传医学研究中心的首席研究员,也是这项研究的资深作者。
“脂肪堆积成为成核事件,导致患者肌肉功能突然下降。这项关于LGMD2B疾病的新观点开启了以前未被意识到的干预途径,”该研究的主要作者Marshall Hogarth博士补充说。
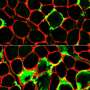
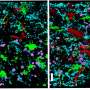
由Jaiswal领导的研究团队与西班牙巴塞罗那巴塞罗那的医院Gallardo和Jordi diaz Manera合作,从患有轻度至严重症状的LGMD2B的人中检查肌肉活检。他们发现脂肪型沉积物起源于肌肉纤维之间的细胞外基质空间,积累与疾病严重程度相关的程度。他们发现肌纤维在缺陷型实验模型中预测疾病严重程度的脂质积累的类似渐进性增加。更重要的是,这种过程可以通过肌肉损伤加速,触发增加的区域中的脂肪植物替代品,否则将被肌肉细胞占据。
“fap的积累和成脂分化是导致铁蛋白异常肌肉功能下降的原因。逆转这一趋势可以为LGMD2B提供一种治疗方法,LGMD2B是一种没有有效治疗方法的毁灭性疾病,”Jaiswal预测,该团队继续在这一领域进行研究。
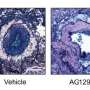
承诺的现成药物包括BATIMASTAT,一种抑制细胞外基质酶基质金属蛋白酶的抗癌药物。该药物在体外减少FAP脂肪生成,减少体内伤害引发的脂质形成。在实验模型中,BATIMASTAT也增加了肌肉功能。
进一步探索








用户评论