揭示了导致成瘾抗性的分子机制
吉尔·特纳(Jill Turner)在西弗吉尼亚州长大,她亲眼目睹了毒瘾造成的严重破坏。
“我有很多朋友前途无量,前途无量,”南卡罗莱纳药学院的助理教授说,“但他们不是吸毒过量就是因为毒品相关的东西进了监狱。”这是我去的原因之一药物成瘾研究”。
特纳一直在研究导致人类上瘾的基本生物分子之一:mu-阿片受体。它是人体内的一种蛋白质,会受到许多不同药物的影响,从尼古丁到酒精再到海洛因。
这种阿片类受体蛋白的一个特别有趣的方面是,它的组成中看似很小的变化可以对它所组成的生物的许多行为产生戏剧性的影响。每一种蛋白质都是由许多称为氨基酸的亚基组成的,其中一个氨基酸的变异有时就意味着整个生物体的巨大变化。
只有有限数量的氨基酸——大约20种——被用来构建蛋白质,而蛋白质通常有几百个氨基酸长。蛋白质就像马赛克一样是由氨基酸。细胞有20种“颜色”可供选择,一个蛋白质有几百个“像素”,从某种意义上说,细胞构建了一个蛋白质的马赛克,具有独特的图像。
仅仅改变普通拼接中的一个像素就会得到非常相似的图像,也许第一眼看起来是一样的。然而,在生物分子的世界里,单是对mu-阿片受体组成的一个改变就会产生巨大的影响。
在人类中,有两种相对常见的μ -阿片受体,它们只因一种氨基酸而不同,这种氨基酸有时被称为A变体和G的变体。在白种人中,G变异只占人口的5%到15%。特纳说,人口研究仍然相对较新,但具有这种变异的个体与其行为之间的一些联系正在变得清晰起来。携带这种蛋白质G变异的人更容易戒烟。他们不容易酗酒。他们不太可能对海洛因上瘾,而且更容易戒除毒瘾。作为孩子,他们似乎在面对压力情况时更有弹性,比如受到长辈的虐待或欺凌。
特纳着迷于这种复杂的人类行为可以被一个氨基酸改变。这种蛋白质的差异源于DNA中的一个单一差异:拥有这种蛋白质G变体的生物体被称为拥有G等位基因。
特纳说:“至少对我自己来说,很难想象你dna中的一个变化——一个点,一个核苷酸——会有这样的影响。”“它是如何转化为行为、社会反应和寻求快乐的巨大变化的?”
她的实验室已经深入研究了这一过程的分子细节。她的团队最近在该杂志上发表了一篇论文神经药理学,他们解决了研究人员一直在问的一个基本问题,即具有A和G变体的个体之间的差异:它是由mu-阿片受体数量或功能的差异引起的吗?
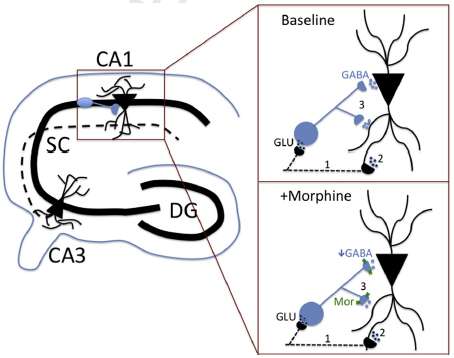
研究人员使用了一种动物模型,该模型被证明可以复制与人类相似的成瘾行为,并将两种变体的个体进行了比较。他们发现了G变异在海马体中产生一种不同类型的神经系统的证据,海马体是大脑的一个基础结构。
例如,在G变体中,加入吗啡后,海马微电路中的反应减弱。Turner说,另一种假设——G变异引起的差异是在那里表达的蛋白质数量减少的结果——没有被断然否定,但是阿片类受体功能丧失的证据是强有力的。
增加了关于阿片受体她补充说,这将增加已经存在的个性化医疗的临床潜力。
特纳说:“如果有人酗酒,你不需要测试这些基因变异,也不需要给病人服用纳曲酮之类的药物来帮助控制酒瘾。”“然后他们回来找你,又旧病复发。如果你在给他们药物之前对他们进行基因分型,你就会知道你应该给他们其他的东西。他们需要一种不同的药物。
“这就是药物基因组学的整个理念,真的很酷。”
进一步探索











用户评论