研究表明基因肝脏疾病的潜在治疗目标
西北医学调查人员已经发现了一种罕见的基因突变的分子机制,增加严重肝脏疾病的风险,根据研究结果发表在分子细胞。
领导的研究中,方得雨,博士,Hosmer艾伦约翰逊病理学教授,可以揭示潜在的治疗靶点治疗这种疾病。
alpha -抗胰蛋白酶(AAT)缺乏症是一种罕见的基因突变,可以增加患一些疾病的风险,包括严重肝疾病。每3500人中有一个人在美国每年诊断出患有遗传障碍。
AAT蛋白质是由肝脏和进入血液保护肝脏及其他器官免受感染。AAT不足,然而,可能导致低水平的AAT在血液和肝脏中蛋白质的积聚,可危及生命。
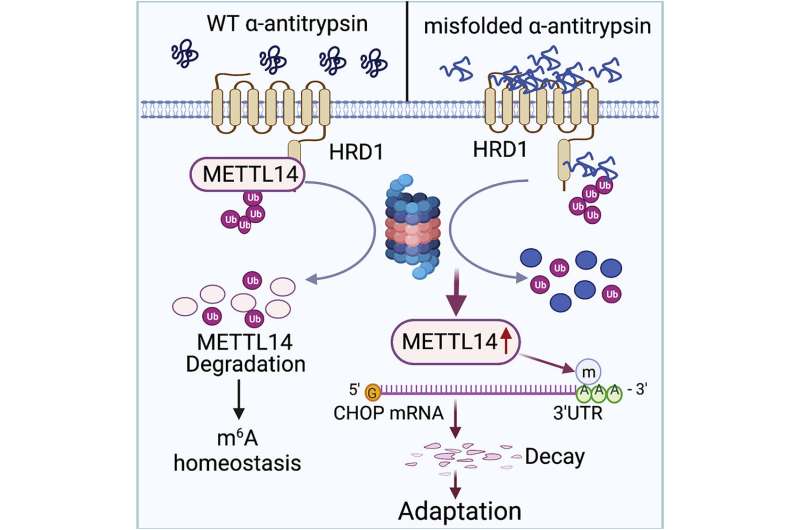
AAT缺陷是由突变引起的丝氨酸蛋白酶抑制剂1 (SERPINA1)基因,产生体。在分子尺度,突变导致有毒的蛋白质积累hepatocytes-specialized内质网内肝细胞——触发一个展开的蛋白质反应细胞应激适应。
展开的蛋白质反应是至关重要的,恢复细胞的正常功能通过阻止蛋白质翻译、降解错误折叠的蛋白质和细胞信号通路激活有益。展开的蛋白质反应的失败,然而,凋亡,或细胞死亡,以及破坏周围组织或器官,肝脏。
的分子机制确定这个展开的蛋白质反应选择压力适应在细胞凋亡仍然未知。
在当前的研究中,方舟子和他的同事利用免疫荧光研究肝细胞系AAT-induced肝脏疾病的小鼠模型。
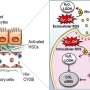
他们发现的蛋白质的积累调节代谢酶N6-adenosine-methyltransferase-14的表达,或METTL14小鼠模型。METTL14也抑制C / EBP-homologous(切)对内质网应激适应protein-induced细胞凋亡。
“小鼠肝脏特定METTL14删除极易受急性药理和AAT deficiency-induced内质网proteotoxic压力和肝损伤,”方说。
研究人员然后越过METTL14基因敲除小鼠模型与控制AAT-induced肝脏的小鼠模型疾病基因敲除小鼠模型,发现仅存活了14周。这表明的删除切蛋白质保护METTL14从proteotoxic基因敲除小鼠肝损伤,根据作者。
进一步探索