研究人员发现了家族性肌萎缩性侧索硬化症患者神经元死亡的原因
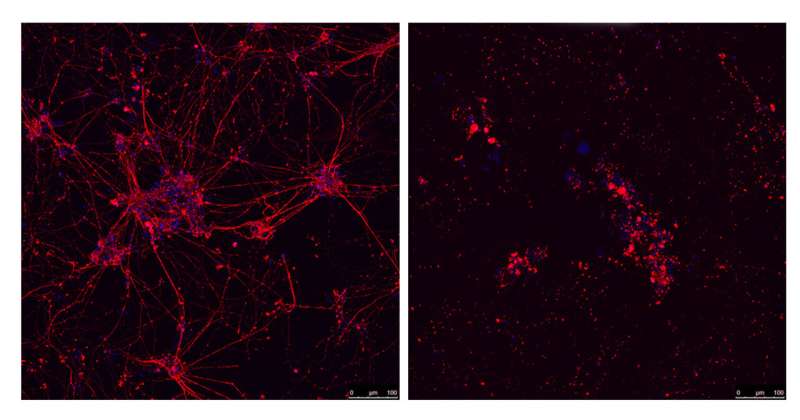
在肌营养的侧面硬化症(ALS)中,控制身体运动的神经元的渐进死亡导致肢体中的肌肉瘫痪,逐渐成为全身的渐变,这最终使其无法呼吸。ALS目前无法治愈,其原因是未知的。
然而,已知的是,在10%的受感染个体中,有一种强烈的遗传成分导致该疾病在一个家族的几个成员中发生。在这些家族性肌萎缩性侧索硬化症的病例中,大约有一半源于一种名为C9ORF72的基因。但是为什么这个基因的突变会杀死运动神经元呢?
西班牙国家癌症研究中心(CNIO)领导的基因组不稳定组现在发现了一种机制,解释了C9ORF72中突变的毒性。新颖的机制将这些突变链接到阻止所有的一般问题核酸,DNA和RNA,因此破坏了对细胞功能的基础的多种方法。
本文本周发布盟军杂志CNIO研究人员Vanesa Lafarga和Oleksandra Sirozh为第一作者。
为什么渐冻症患者的神经元会死亡
Als研究人员已经观察到,许多使用核酸在受影响患者的神经元中失败的许多基本细胞过程。现在,CNIO组提供了一种连接它们的模型,并解释了这些广泛的问题。
Fernández-Capetillo说:“我认为我们有一个非常令人满意的模型,它帮助我们了解肌萎缩性脊髓侧索硬化症患者的运动神经元中发生了什么,是什么杀死了他们。”“我们很兴奋,因为治愈任何疾病的关键是首先了解什么没有起作用。只有这样,你才能开始寻找治疗方法。”
尽管新发现的机制与特定基因中的突变相关C9ORF72,但CNIO组认为其他与之相关的突变可能以类似的方式作用,即通过阻断运动神经元的DNA和RNA。
太多的精氨酸
CNIO研究人员揭示了C9ORF72基因中的突变,因为它们诱导细胞产生非常富含精氨酸,氨基的小蛋白质或肽。氨基酸因此,由于其正电荷和化学性质,近期杀死核酸,DNA和RNA。
CNIO的研究表明,这些富含精氨酸的蛋白质以如此高的亲和力与核酸结合,广泛地取代了所有与DNA和RNA相互作用的细胞蛋白质,从而阻断了任何涉及DNA或RNA的细胞反应。结果,由于其核酸被有效阻断,细胞死亡。
DNA包含细胞制造正常功能所需蛋白质的指令。数以百计的蛋白质需要将自己固定在DNA和RNA上,以阅读它们的指令,并最终为细胞制造新的成分。但是,这项新研究的作者补充说,“富含精氨酸的多肽的存在阻碍了与核酸有关的任何反应。”
Fernández-capetillo说:“我们所看到的是含精氨酸的肽就像一种粘附在核酸上并装饰它们的一种焦油,并且在这样做时,它们使通常与核酸结合的蛋白质置换为此什么都没有涉及DNA或RNA工作。“
尤里卡时刻
“在所有这些研究的研究中,神经科学研究人员一直在使用核酸的反应中出版各种问题:翻译,复制等。无所事事!我们认为我们的模型给出了所有这些观察的简单答案,”仍然是fernández-Capetillo。
Fernández-Capetillo的研究通常集中在癌症上,但他努力关注任何可以应用他的知识的问题。2014年,他开始研究肌萎缩性侧索硬化症(ALS)。他确信,他的团队最近建立的一项技术可以帮助他们了解C9ORF72基因突变的毒性。正是他的灵光一闪,和诺贝尔奖得主杰克·绍斯塔克在CNIO喝咖啡后产生的想法,让他找到了精氨酸。
“绍斯塔克研究了生命起源的化学过程,他告诉我为了停止与核酸有关的反应,他们在实验中使用了含有大量精氨酸的合成肽,因为精氨酸与核酸的亲和力很高,”Fernández-Capetillo说。“所以我想,如果这就是发生的事情,如果肌萎缩性侧索硬化症患者体内富含精氨酸的蛋白质以一种普遍的方式阻止了DNA和RNA呢?”
紧致精子核心的蛋白质是相同的
当该组决定在细胞暴露于自然时也看到是否看到类似问题时,支持这个初步假设蛋白质有很多精氨酸。存在这样的蛋白质,但在精子细胞的发育过程中仅瞬时表达:protamine。
与现在发布的模型一致盟军杂志,鱼精蛋白的生物学功能是将组蛋白从DNA中取代;组蛋白是促进DNA压缩的蛋白质。“通过用组蛋白交换鱼精蛋白,鱼精蛋白更小,精子DNA可以变得更紧密,”Fernández-Capetillo解释道。
然而,protamine对不是精子细胞的任何细胞有毒。“我们认为在ALS患者中发生的是相当于如果他们的运动神经元意外开始产生protamine会发生什么。”
的确,纸张里面盟军杂志表明,protamine的细胞效应与ALS患者中发现的精氨酸富含肽的细胞效应相同。
如何克服毒性
现在,该集团已确定为什么精氨酸丰富的肽有毒,下一步是找到克服这种毒性的方法。沿着这些线路的研究已经开始在本集团中。作为制造动物模型的作品,其中存在问题 - 再现有毒肽的生产,以提供用于测试潜在疗法的平台。
学习如何缓解这些肽的毒性也可用于解决非C9ORF72相关的ALS,即整个疾病。论文的作者认为,核酸阻断的广泛机制可能是als中发生的事情。
Vanesa Lafarga说:“在肌萎缩性侧索硬化症患者中发现的绝大多数突变发生在结合RNA的蛋白质中,而这些突变通常会阻止这些蛋白质与RNA的结合。此外,这些患者的细胞也有非常普遍的问题与他们的核酸。这就是为什么我们认为,虽然C9ORF72的突变只影响部分渐冻人,但神经元毒性的机制可能与其他渐冻人没有本质上的不同。我们现在正在努力证明情况是否如此。”












用户评论