资料来源:CC0公共域名
来自剑桥大学、米兰大学和谷歌Research的研究人员利用机器学习技术预测蛋白质,特别是与神经疾病有关的蛋白质,如何在几微秒内完全改变其形状。
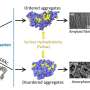
他们发现β淀粉样蛋白,一个关键蛋白与阿尔茨海默氏症有关联,它的形状非常混乱,实际上它变得不太可能粘在一起,形成导致脑细胞死亡的有毒簇。
研究结果发表在该杂志上自然计算科学这可能有助于未来蛋白质紊乱疾病的治疗,如阿尔茨海默氏病和帕金森氏病。
剑桥错误折叠疾病中心的Michele Vendruscolo教授领导了这项研究,他说:“我们习惯于认为蛋白质是折叠成定义明确的结构的分子:找出这一过程是如何发生的是过去50年的主要研究重点。”“然而,我们体内大约三分之一的蛋白质没有折叠,而是保持无序的形状,有点像汤里的面条。”
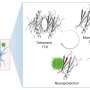
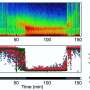
我们对这些无序蛋白质的行为了解不多,因为传统的方法倾向于解决确定静态结构的问题,而不是运动结构。研究人员开发的方法利用谷歌的计算机网络来产生大量的短轨迹。最常见的运动在这些“电影”中多次出现,这使得定义无序蛋白质在不同形状之间跳跃的频率成为可能。
“通过计算这些运动,我们可以预测哪些状态蛋白质剑桥大学尤瑟夫·哈米德化学系的第一作者托马斯·Löhr说。
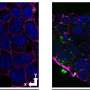
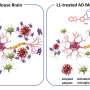
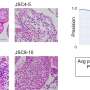
研究人员将注意力集中在β淀粉样蛋白肽,一种与阿尔茨海默病有关的蛋白质片段,它聚集形成淀粉样斑块在受影响个体的大脑中。他们发现,β淀粉样蛋白每秒在不同的状态之间跳跃数百万次,而不会在任何特定状态下停止。这是疾病的标志,也是迄今为止贝塔淀粉样蛋白被认为是“不可用药”的主要原因。
“贝塔淀粉样蛋白的持续运动是它很难被定位的原因之一——这几乎就像试图在你的手中捕捉烟雾,”Vendruscolo说。
然而,通过研究β淀粉样蛋白的变异,其中之一氨基酸通过氧化改性,研究人员了解了如何使其抗聚集。他们发现它被氧化了淀粉样蛋白Beta改变形状的速度甚至比它的未修改的对手更快,这为解释氧化版本的聚集倾向降低提供了一个理论基础。
“从化学的角度来看,这种修饰是一个微小的变化。但是它们之间的状态和转换的影响是剧烈的,”Löhr说。
“通过使无序的蛋白质更加无序,我们可以防止它们以异常的方式自我联系,”Vendruscolo说。
该方法为研究一类快速无序运动的蛋白质提供了一个强大的工具,尽管它们在生物学和医学上很重要,但迄今为止仍是难以捉摸的。
更多信息:Thomas Löhr等,阿尔茨海默氏病Aβ肽的动力学集合,自然计算科学(2021)。DOI: 10.1038 / s43588 - 020 - 00003 - w
期刊信息:自然计算科学
所提供的剑桥大学