淋巴瘤是不同的路线
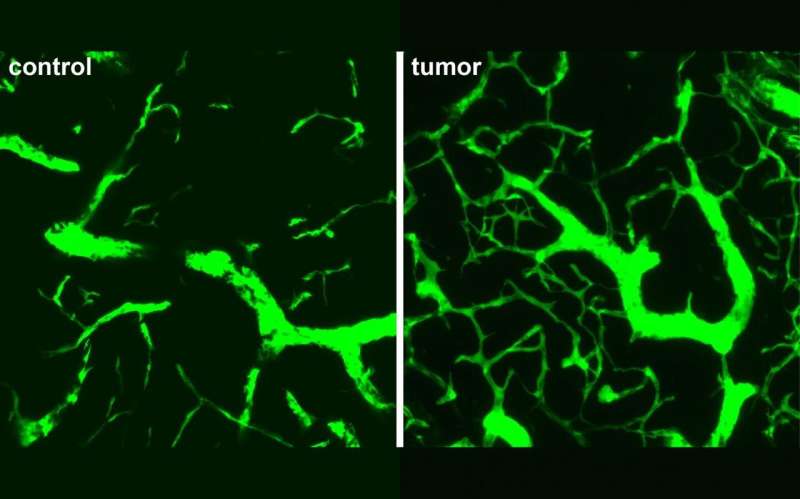
创建新的血管,这一过程被称为血管生成,肿瘤的淋巴结是不同的比身体的其他部位的肿瘤,如结肠或肺,一个团队从马克斯Delbrueck分子医学中心的亥姆霍兹联合会(MDC)在《华尔街日报》报道癌症研究。争取民主变革运动的实验室的科学家阿明雷姆曾为此写过博士博士Uta Hopken Holger格哈特教授参与了这个项目。团队标识可能更有效的治疗目标为淋巴瘤患者肿瘤生长缓慢。
淋巴瘤是淋巴系统的癌症,包括淋巴结、脾和骨髓。淋巴瘤患者增加血管发展的指标通常有较低的生存机会。他们还不反应良好的治疗,已经成功地抑制血管发展其他类型的癌症。
“我们假设肿瘤淋巴结是完全不同于实体肿瘤,因为淋巴结为血液承担提供这种支持的微环境肿瘤细胞负责人博士说:“Uta Hopken MDC的自身免疫微环境调控和癌症实验室。不过,这是“绝对奇怪,没有通常的嫌疑人,“阿明雷姆曾为此写过博士说,领导争取民主变革运动的平移Tumorimmunology实验室。
消除怀疑
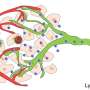
血管早期淋巴瘤异常密集和不规则,比观测到的更多的分支血管的健康的淋巴结。分支的模式没有被观察到实体肿瘤在发展中器官感染淋巴结或,通常neo-angiogenesis的其他网站。
发现独特的信号通路,推动这一发展,分析利用转基因小鼠模型,开发团队在淋巴瘤,以及植入小鼠淋巴瘤癌症细胞。他们看着基因表达模式看到哪些基因和蛋白质是最活跃的肿瘤发展的初始阶段。
罪犯通常涉及肿瘤angiogenesis-inflammation,低氧水平和血管的基础和技巧之间的信号,称为缺口signaling-did不会显示在结果中。
成功的块
的一组蛋白质,叫做血管内皮生长因子(VEGF),被认为是正常的主要驱动因素血管的发展,以及在肿瘤血管生成。在大多数固体肿瘤,VEGF-A蛋白质调节过程,结合受体,称为VEGFR-2。
在淋巴瘤的早期阶段中,团队发现VEGF-C最活跃的蛋白质。当他们试图阻止受体VEGFR-2抑制VEGF-C活动,没有什么改变。
但是当研究人员阻止了不同的受体,VEGFR-3,血增长明显放缓。他们也打断了一种叫做淋巴毒素的蛋白质受体,通常需要正常淋巴结发展,也有助于减缓血管生成。
该团队使用两种药物已经批准临床使用在自身免疫性疾病抑制途径。他们也证实治疗工作人类细胞。虽然不是医生,研究人员希望可以采取治疗的临床试验来研究其有效性在人类患者。“如果一些癌细胞生存化疗,有可能防止复发通过解决这些途径免疫疗法,“雷姆曾为此写过说。
从一开始看
本研究的一个关键特性是时机。研究人员追踪血管生成在肿瘤细胞入侵后的第一个12天淋巴结。这给了他们一个独特的机会去观察“相声”或早期肿瘤细胞和淋巴结微环境之间的相互作用。只有5 -百分之十的淋巴结细胞癌变,并且已经淋巴结被重组。“我们看到的变化是早期发生的肿瘤负荷很低,“Hopken说。
高分辨率成像这些早期的变化提出了一个挑战,需要大量的努力。“淋巴瘤细胞中广泛分布的细胞高度区分淋巴结,”Lutz门泽尔说,co-first作者在平移Tumorimmunology实验室和博士后。“寻找lymphoma-induced基质重塑,当其他区域的淋巴结仍未受影响,经常成为寻找“针”在显微镜下。”
团队强调动物为这项工作的重要性。这样的研究是不可能与人类患者,因为他们还没有表现出症状。“动物提供的优点看发生了什么疾病的开始,而不是结束,”雷姆曾为此写过说。“瀑样只是远远不够发达模仿许多不同的细胞类型之间的交互复杂的淋巴结组织。”
该集团计划继续调查之间的关系肿瘤细胞和淋巴结微环境,看看单细胞测序可以揭示更多关于血管生成过程。
进一步探索