专家在实验性阿尔茨海默病药物急剧分裂
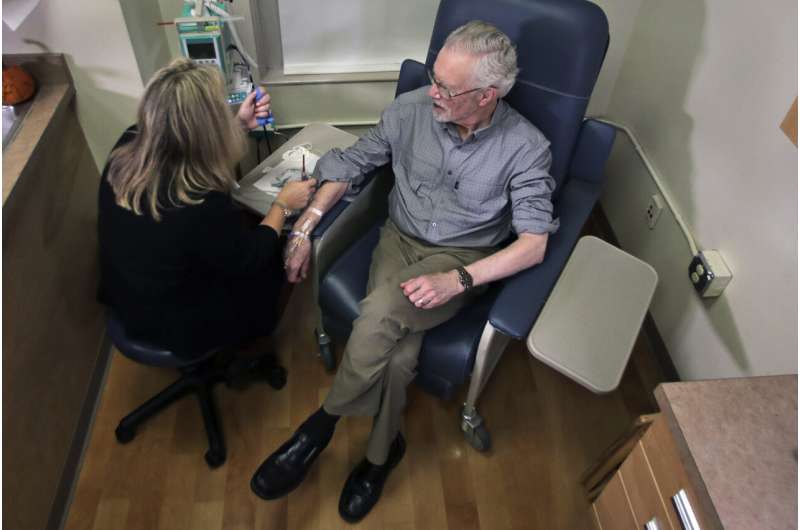
公司声称第一个从阿尔茨海默病药物减缓智力下降了案件大幅科学家周四但让他们分歧是否有足够的证据有效性的医学,联邦政府的批准。
兴奋和怀疑包围aducanumab以来开发商停止今年早些时候的两项研究,因为它似乎没有工作,然后做了一个惊人的大变脸,说10月新结果表明它是有效的高剂量。
在周四的演讲在圣地亚哥召开的一个阿尔茨海默氏症,开发商让一些专家相信药物值得认真考虑。但是其他人都是可疑的。
更改在研究和不同寻常的分析的数据结果很难解释。和新发布的结果显示,药物只是一个很小的差异思维能力在一项研究中,没有其他。
老年痴呆症患者和家庭急需任何帮助,无论多小,美国食品和药物管理局批准增加压力。
但与冲突的结果,“我看不出你如何可以得出任何其他比另一个需要做试验,”梅奥诊所的David Knopman博士说,曾参与的一个研究。
劳里瑞安痴呆国家老化研究所的科学家,同意:“我们需要更多的证据。”
其他医生咨询药物开发者欢呼的结果。老年痴呆症专家保罗·爱森博士在南加州大学,说他们是在给他们带来利益的一致的和积极的“高剂量——“一个真正的重大进步。”
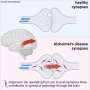
Aducanumab旨在帮助身体清除有害的斑块,或蛋白质团,从大脑。马萨诸塞州剑桥的一家生原体与日本卫材公司的发展。
在下午的交易中,这些公司的股票上涨了约4%。
批准或拒绝的风险很高。
超过500万人在美国和全球数以百万计的阿尔茨海默氏症。当前药物只是暂时缓解症状,不慢记忆和思维能力的丧失。

但批准一种不是真正有效的药物可以使病人减少金融和医疗风险和给其他制药公司激励发展更好的治疗方法。
aducanumab的制造商进行了两项研究,每个招收大约有1650人患有轻度认知障碍或轻度痴呆阿尔茨海默氏症。
那些有疾病的基因,提高他们的风险开始在低剂量,因为他们更容易患脑部炎症从药物目标斑块。
但随着研究继续关注这个副作用有所缓解,规则改变了,让这类患者得到更高的剂量。
一个副总裁,萨曼莎·巴德Haeberlein说,更多的人得到了高剂量在一项研究中,这有助于解释为什么它成功了,而另一个失败了。

但新的分析部分结果,方法一开始就不同意,这使得任何结论不可靠,独立专家说。
另外,药物的好处可能看起来比他们真的更令人印象深刻的,因为病人安慰剂组恶化更多实证研究的失败。
“很难确切地知道发生了什么,”霍华德的事博士说,首席科学官阿尔茨海默氏症的药物发现的基础。“我不认为FDA如何批准。”
问题也出现了大小的任何好处。
药物没有扭转下降,只是放缓的速度相比安慰剂组22%在一项研究中。然而,这意味着只有0.39的差异思维技能的18分。
“这是一个非常小的量,”沉默说的。
玛丽亚Carrillo,首席科学官阿尔茨海默氏症协会说,这是“迄今为止最大的减少,我们已经看到,”并补充说:“这可能意味着他们记住他们的亲人一会儿。”
药物“值得重要的、严格的探索”和FDA审查,她说。“这是阿尔茨海默氏症社区的一个重要时刻。”
一些医生和病人测试药物确信它帮助。
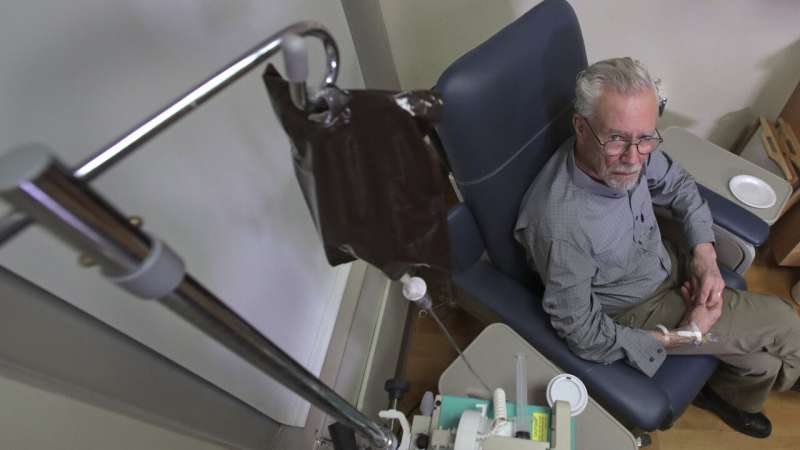
查尔斯兴,78年,一位退休的部长詹姆斯敦,罗德岛,接受aducanumab直到3月停止了研究。自从他被抬下了药,”他的认知,他的警觉性,肯定他的互动减少,“说他的妻子辛西娅兴。
生原体强调需要一个有效的治疗方法,建议推迟访问的药物可能会剥夺许多人的帮助,正做进一步的研究。
-

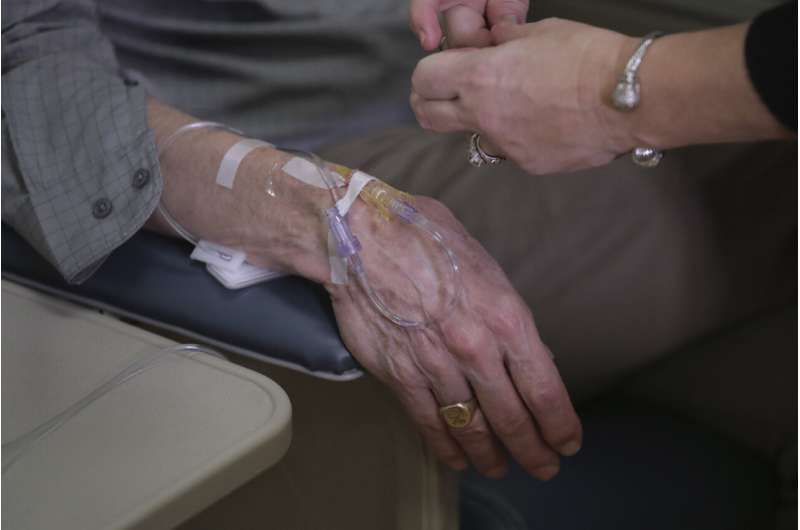
在这个2019年11月22日,照片,查尔斯•弗拉格受损与阿尔茨海默氏症,使一个花生酱三明治家里吃午饭在詹姆斯敦,R。我兴药物Aducanumab参与研究。新结果公布实验医学的制造商声称它可以减缓老年痴呆症的衰落,最常见的痴呆症。(美联社照片/查尔斯·Krupa) -

在这个2019年11月22日,照片,查尔斯•弗拉格受损与阿尔茨海默氏症,使一个花生酱三明治在詹姆斯敦家里吃午饭,也是兴是药物Aducanumab参与研究。新结果公布实验医学的制造商声称它可以减缓老年痴呆症的衰落,最常见的痴呆症。(美联社照片/查尔斯·Krupa)
斯坦福大学的专家约翰·埃尼迪斯博士在研究方法上,说病人的需要不应该开车FDA的决定。
“如果我们沿着这条道路,我们很可能会引入大量的无效治疗疾病很常见,”他说。“这将会一团糟。”
©2019美联社。保留所有权利。