研究人员解决了一个关于细胞部门如何被拨打的谜团

一支国际研究人员已经确定了一种功能,如流变垫,通过脱落作为偏离开关的肿瘤抑制蛋白来拨打细胞分裂。该机制提供了洞察力的洞察力,导致癌症的细胞增殖。
该研究的重点是内在紊乱的蛋白质P27。蛋白质有助于调节细胞分裂通过整合分子信号这导致P27自己的退化和细胞分裂的开始。低水平的p27与a相关联预后差在乳房,前列腺,结肠等癌症。降解p27的切换机制在某些白血病和乳腺癌中上调。
本月在期刊上发表的研究自然通信揭示了即使当P27在含有必需细胞分裂蛋白的复合物中紧密结合时,P27的小区段在边界和局部未结合的结构之间不断波动。波动使信号分子能够放松P27与之相关的访问蛋白质复合物及其最终的去除和退化。
这项工作由科学家们在德国Heinrich-Heine-University的ST. Jude儿童研究院的科学家领导,比利时Vrije University Brussel。
“本研究中捕获的P27中的波动可能是由p27这样的调节内在蛋白质信号传导的一般机制。这些是我们所知道的蛋白质可以被颠覆癌症和其他疾病,”博士克里沃克·博士议员称。,圣裘德结构生物系的成员。另一位相应的作者是Vije University Brussel博士学位的彼得汤姆PET博士,博士,佛罗里达州布鲁塞尔博士,博士,博士,博士议员在海因里希 - Heine-大学。
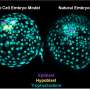
本质无序的蛋白质
蛋白质是串上的氨基酸样珠阵列 - 最常折叠成稳定的3-D结构以进行其功能。而不是形成稳定的结构,P27就像剩下完全或部分紊乱的所有蛋白质的三分之一到一半。本机紊乱的蛋白质可以根据需要迅速改变形状以满足重要细胞功能。
挑战一直在弄清楚P27如何在细胞分裂的背景下履行该角色。研究者知道从蛋白质复合物中移位P27,涉及磷酸化特异性P27氨基酸。以前的工作表明,这些氨基酸无法进入,而P27与细胞分裂蛋白结合。
调查人员从单分子荧光综合数据以及结构,生化和生物物理方法,以捕获P27中的波动。研究人员称此过程动态预期。“在蛋白质复合物中,P27波动在可能的磷酸化的主要结合和部分释放状态之间,”Kriwacki说。“该研究说明了用于揭示这种构象开关机构的细节的单分子荧光方法的力量。”
在Kriwacki实验室的共同作者Aaron Phillips,Ph.D.中:“通过这种结果,它变得越来越明显,许多蛋白质,甚至结构化蛋白质,经历了重要的构象波动,这对其功能至关重要。”
进一步探索










用户评论