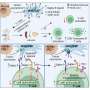
第二个“别吃我”的信号上发现癌细胞
第二个生物通路信号免疫细胞吞噬和杀死癌细胞被研究者在斯坦福大学医学院。
抗体只会“不要吃我”的信号表明承诺作为癌症治疗在动物模型中,目前正在临床试验。结合抗体,称为cd47抗体,与另一块这个新发现的途径可能会进一步增强免疫系统能力,消除许多类型的癌症,研究人员认为。
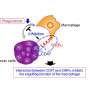
“癌细胞的发展引发的生成SOS分子被身体的巨噬细胞,被称为巨噬细胞欧文·韦斯曼说,医学博士,主任斯坦福干细胞生物学和再生医学研究所和路德维希癌症中心。“然而,侵略性癌症表达“别吃我”的信号的形式CD47表面。现在我们已经确定了一个“别吃我”的信号及其互补受体在巨噬细胞。我们还表明,我们可以克服这个信号与特定的抗体和恢复巨噬细胞杀死癌细胞的能力。”
有一篇描述该研究结果在线发表在11月27日自然免疫学。斯曼,病理学教授和发育生物学,股票研究的高级作者罗伊Maute与前博士后学者,博士,现在从头开始生物学主管Biotherapeutics Inc .研究生阿米拉Barkal股票铅作者与前研究生Kipp Weiskopf,医学博士,博士,现居住在布莱根妇女医院。
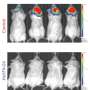
“同时阻断这些途径在小鼠体内导致肿瘤的浸润与许多类型的免疫细胞,显著提升肿瘤间隙,导致较小的肿瘤总体而言,“Barkal说。“我们正兴奋的可能性两倍——或者甚至triple-pronged治疗人类癌症我们结合多个封锁增长。”
巨噬细胞的重要性
巨噬细胞是巨大的白细胞发现在几乎所有身体的组织。的一部分,所谓的先天免疫系统,他们吞噬并杀死外来入侵者如细菌或病毒。他们也摧毁死亡细胞和,在某些情况下,肿瘤细胞的内部发展线索已经乱了套。
“不要吃我”的信号被确定在2009年斯曼的实验室。他的团队发现,几乎所有肿瘤细胞表达高水平的分子称为CD47表面。他们表明,CD47蛋白结合SIRPalpha巨噬细胞表面,抑制他们杀死癌细胞的能力。
动物研究表明,治疗一个cd47抗体抗体大大改善了巨噬细胞杀死癌细胞的能力,甚至导致了一些治疗癌症的小鼠模型。第一期临床试验正在进行中在斯坦福大学,在英国测试治疗的安全性和有效性在人类各种各样的血液和实体肿瘤。
新发现的绑定交互使用的癌细胞逃避巨噬细胞利用癌细胞的蛋白质结构的表面称为“主要组织相容性复合体类1,或MHC类1。人类肿瘤的表面有高水平的MHC类1更耐cd47抗体水平较低的治疗比复杂,研究人员发现。
适应性免疫的
MHC类1是适应性免疫的一个重要组成部分,第二个主要的免疫系统,依靠免疫细胞T细胞和B细胞机敏地特别是应对外国入侵者和细胞损伤。身体的大多数细胞表达MHC一班的表面作为一种不加选择地显示的许多蛋白质中发现计算单元a细胞的内部结构的随机抽样,它提供了一个窗口的健康和功能。如果蛋白质碎片,称为肽MHC所显示异常,T细胞破坏细胞。尽管MHC类之间的关系1和已经成熟的T细胞,这是不清楚以及复杂与巨噬细胞相互作用。
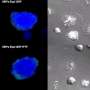
Barkal和她的同事们发现,一种叫做表面LILRB1巨噬细胞的蛋白质结合MHC一班的一部分在癌细胞广泛共享的个人。这个绑定抑制巨噬细胞的吞噬能力和杀死癌细胞,当越来越多的在实验室菜和老鼠与人类肿瘤,研究人员发现。抑制CD47-mediated通路和LILRB1通路显著减缓小鼠肿瘤的生长。
理解之间的平衡适应性和先天免疫在癌症免疫治疗是很重要的。例如,它并不少见,减少人类癌症细胞MHC的水平1级的表面逃脱毁灭的T细胞。这些类型的肿瘤患者可能是可怜的候选人对癌症免疫疗法旨在刺激T细胞活动与癌症。但是这些细胞可能特别容易受到cd47抗体治疗,研究人员认为。相反,肿瘤细胞与健壮的MHC类1的表面可能不太容易cd47抗体。
“在某些癌症,MHC类1表达,因为各种各样的原因,没有减少,“斯曼说,“这可以帮助癌症细胞逃离巨噬细胞。这些发现帮助我们理解许多方面癌症细胞可以逃避巨噬细胞,我们该如何阻止这些逃生通路。”
“事实上,至少有两个冗余机制来调节巨噬细胞活动证明了是多么至关重要的严格控制我们的免疫反应,“Barkal说。“可能是未来的研究将确定这些途径,这将给我们额外的目标癌症免疫疗法。"
更多信息:MHC类的接触我的抑制性受体LILRB1抑制巨噬细胞和癌症免疫疗法的目标,自然免疫学(2017)。nature.com/articles/doi:10.1038 / s41590 - 017 - 0004 - z