酶的冷冻框架在行动有一个新的癌症治疗概念的含义
经过数百万年的进化,细胞已经发展出了无数种调节过程的方式,使它们能够茁壮成长。特别有用的工具被保存下来,或者说是“保存”了千万年来,所以今天我们可以在广泛的生命形式中找到它们,从最原始的到最复杂的。
2017年7月3日发表的研究通过冷泉港实验室(CSHL)的结构生物学家(CSHL)揭示了一种这种保护机制如何工作,具有对新癌症药物的发展的影响。
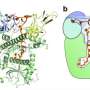
由CSHL教授和Howard Hughes Medical Institute Investigator Leemor Joshua-tor,使用X射线晶体学捕获相当于一类称为Tutases的酶的冻结框架。在分辨的单个原子的情况下,这些图片显示它们与其他分子相互作用以调节称为Let-7的重要小RNA分子的活性。
Let-7是一种microRNA,是发育过程中重要的基因调控因子。当在人类身上表达时,这是我们的干细胞分化成各种特殊的细胞类型,填充我们的器官。在干细胞保持其“干细胞性”(能够无限增加更多干细胞)非常重要的情况下,let-7需要失活。
Let-7具有特殊的意义,因为有些人认为它在癌细胞中的失活导致了这些细胞干细胞的特性可以无限增殖。这将注意力集中在了解调节let-7是活跃还是不活跃的机制上。
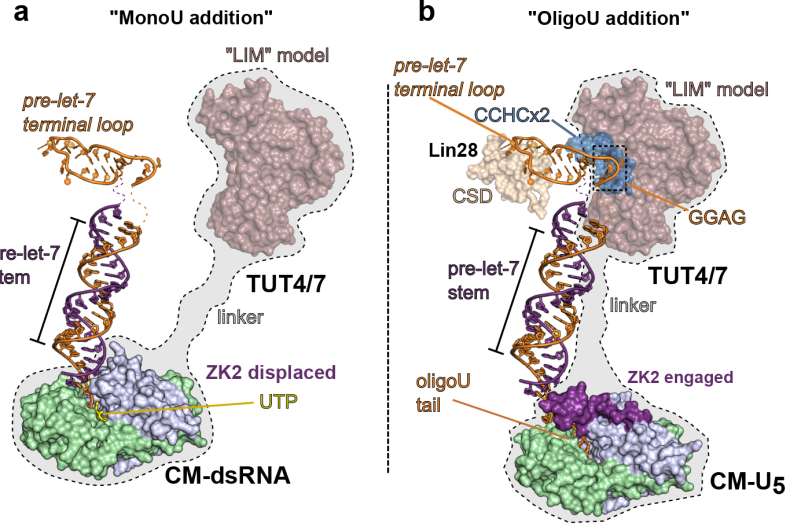
该团队的照片显示了TUT4和TUT7——TUTase的两种酶——在两种环境下的不同作用。在分化细胞中,TUTases纠正了许多let-7前体序列中一个小的遗传缺陷,使成熟的let-7 microrna得以生成。当TUTase在let-7前体的序列上添加一个尿苷分子(“u”)时,这些缺陷得到了改善。
在一个注定要保留其干细胞性的干细胞中,其中一个TUTases在let-7前体上添加了30个尿苷,以这种方式标记它被另一种酶破坏。Joshua-Tor说:“我们已经能够捕捉到这两种不同行为模式的tutase。”
Joshua-tor解释说,辅导是新癌症疗法的有希望的目标。在肾脏和肺部癌细胞例如,当let-7水平远低于正常水平时,标记let-7以进行破坏的TUTases可能会被抑制。拥有它们在分子舞蹈中如何行动的高分辨率图像应该有助于这方面的努力。
“通过TUT4和TUT7控制Let-7生物发生的多域利用”出现了2017年7月3日自然结构和分子生物学。





用户评论