发现机制预测响应在结肠癌新疗法
干细胞和癌症研究小组由赫克托·g·帕尔默博士Vall d ' hebron肿瘤研究所(VHIO)已经确定的分子机制,确定病人的应对某些药物用于治疗结肠癌的临床试验。VHIO也得益于领导的研究与教授合作学院Investigaciones阿尔贝托·穆尼奥斯´s实验室基于Alberto溶胶Consejo优越de Investigaciones Cientificas (IIB-CSIC-Madrid)。今天发表在自然医学,这项工作识别预测生物标志物对治疗的反应,提出治疗方案的病人没有反应。这些进步将引导更好的选择治疗方法,避免使用无效的药物的风险。
结肠癌是一种疾病引起的大肠恶性肿瘤。当早期发现肿瘤切除手术病人接受辅助化疗,消除疾病在大多数情况下。然而,在高级阶段,结肠肿瘤抗广谱的抗肿瘤药物和癌细胞逃避治疗和传播到全身,引起转移。目前还没有有效的治疗方法停止的发展结肠癌在这些后期,大多数病人死于疾病进展的结果。
近年来新药物设计目标和阻止某些分子的活动负责促进肿瘤的生长和转移。其中的一些,目前在临床试验中,在某些患者显示出可喜的成果,而其他人没有改善。这项研究由VHIO微分对治疗的反应,并考察了奥尔加托雷斯基金(FOT),西班牙的科学基础与癌症协会(AECC),卫生和卡洛斯三世研究所(ISCIII)。
新的临床视野
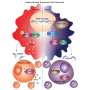
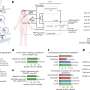
赫克托·g·帕尔默博士´s团队首次描述了致癌基因之间的相互作用的分子机制的Wnt通路/β-连环蛋白和RAS / PI3K / AKT决定响应与药理PI3K和AKT抑制剂治疗。虽然在结肠癌通路都是转基因,这是癌症细胞的细胞核中β-连环蛋白的过度积累使得他们抵抗这些anti-tumoral药物引起的细胞死亡。
PI3K / AKT通路的激活保留FOXO3a蛋白在细胞核外,抑制的能力作为一个肿瘤抑制基因,导致细胞死亡。因此,“针对PI3K和AKT活动与这些小说在细胞核抑制剂允许搬迁FOXO3a促进细胞死亡。这些药物是全球处于临床试验阶段,初步提供的结果在某些肿瘤类型”,赫克托·g·帕尔默解释说,主管VHIO´s干细胞和癌症。
然而,许多结肠癌患者不显示任何好处。这样做的原因是由帕尔默博士解释说:“如果这些抑制剂的患者显示高水平的核β-连环蛋白FOXO3a不能诱导细胞死亡,但通过转义处理促进了相反的效果,导致转移。”According to Héctor Palmer, this finding has tremendous clinical value, since "the identification of nuclear beta-catenin as a biomarker to predict response guides the selection of patients who will benefit from treatment with PI3K or AKT inhibitors and discard their use in candidates who would provoke an adverse response."
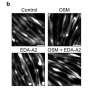
此外,赫克托帕尔默博士和他的同事发现了一个解决方案的患者来说,治疗PI3K和AKT抑制剂是禁忌。他们使用一种实验性药物,减少核β-连环蛋白的水平,允许细胞死亡诱导PI3K和AKT抑制剂。这些发现提出两种抑制剂的组合在未来更有效target-directed治疗结肠癌。
实现个性化医疗的承诺
VHIO先锋功能研究和临床前临床试验在对抗癌症。重要的是,帕默´s博士的团队开发了体内模型,准确地概括结肠癌患者的疾病进展。他们接种动物细胞来自患者的肿瘤,创建一个“xenopatient”模式。这些细胞再生的动物的疾病与个体病人相同的独特的特点,保留原来的遗传、临床和病理改变。xenopatients代表一个平行的现实在实验室中每个病人。这种方法允许研究疾病进展和响应实验药物前让病人新的治疗方法。该模型将很快形成未来功能的基础上,预测和个性化的癌症治疗。