在癌症治疗中通过靶向POLtheta酶阻断DNA生产
BRCA1(乳腺癌基因1)是一种关键基因,在某些情况下会出现缺陷,导致乳腺癌和卵巢癌,它在人体DNA修复机制中发挥着重要作用。BRCA1一旦突变,就会引发癌症。据维也纳总医院家族性乳腺癌和卵巢癌中心称,如果BRCA1或BRCA2基因发生突变,患乳腺癌和卵巢癌的可能性分别增加到85%和53%。
虽然BRCA1和BRCA2的突变支持不受控制的细胞生长,但这些突变也会导致细胞内遗传物质的不稳定。因此,这些类型的癌细胞依赖其他修复机制来补偿这些缺陷。
带有突变BRCA1或BRCA2基因的细胞对其他基因的依赖可以被视为癌细胞的阿喀里斯之踵,因为靶向其他DNA修复基因可以产生合成致死关系。
维也纳医科大学综合癌症中心的副教授、CeMM的前研究小组组长Joanna Loizou解释说:“合成致命性作为治疗乳腺癌和乳腺癌的一个治疗概念卵巢癌特别防止癌细胞分裂同时不影响健康细胞这种治疗理念比传统化疗有优势。”
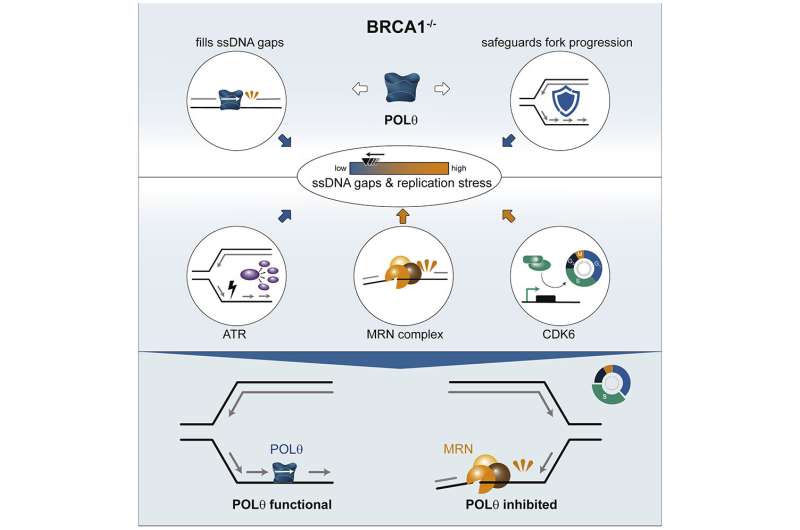
POLΘ填补了单链DNA的空白
该研究的第一作者安娜·施伦普夫(Anna Schrempf)和萨拉·贝尔纳多(Sara Bernardo)关注的是酶POLΘ (DNA聚合酶theta),它是细胞DNA修复机制的一部分,它的丢失在BRCA1突变时是合成致命的。POLΘ已被证明在修复DNA双链断裂中发挥关键作用。
他们的研究发表在细胞的报道,两位研究人员都表明,除了这一作用,POLΘ还填补了DNA复制过程中产生的单链DNA空白。
“我们演示了之前描述过的POLΘ的功能,这让我们更好地了解它的DNA修复机制和它在DNA复制中扮演的重要角色。通过药物抑制POLΘ,我们破坏了BRCA1突变癌细胞的遗传物质的稳定性,进一步减缓细胞分裂并停止生长,”Schrempf解释道。
类似的方法已经被成功采用癌症治疗通过抑制PARP,一种类似于POLΘ-has的蛋白质,与brca1缺陷细胞的合成致死关系。在临床应用中,基于parp的治疗被发现非常成功,但也发现患者产生了耐药肿瘤。
Loizou说:“这使得详细了解我们DNA修复机制的过程,并确定其他潜在的治疗途径变得更加重要。”