缺氧和胎儿血红蛋白之间的联系为镰状细胞病提供了希望
圣裘德儿童研究医院的科学家们表明蛋白质负责适应低氧环境(缺氧),导致胎儿血红蛋白表达增加(住宅)的成年人。这一发现对于治疗镰状细胞病有一定的意义和beta-thalassemia,严重影响数百万人的血液疾病。这项研究发表在今天自然发表在GitHub,相关代码。
血红蛋白是一种蛋白质海绵,吸收氧气和允许红细胞运送到全身。成人血红蛋白包含四个蛋白质subunits-twoβ球蛋白和两个身体里。
β球蛋白的突变导致镰状细胞病和beta-thalassemia。但人类有另一个血红蛋白亚基基因(gamma-globin),这是在胎儿发育的表达而不是β球蛋白。Gamma-globin与身体结合形成住宅。通常在出生,gamma-globin表达式是关闭和β球蛋白,导致从住宅转向成人血红蛋白。
“我们已经知道多年来持续的住宅表现出生后可以减轻镰状细胞病的症状和beta-thalassemia,“通讯作者米切尔·j·维斯说,医学博士博士,圣裘德血液学部门椅子。“和非常高的住宅水平可以治愈这些疾病,尽管β球蛋白基因存在缺陷。因此,许多实验室都集中在了解围产期开关从γ-β球蛋白基因表达并找出新的方法来逆转药物或基因疗法。”
恢复住宅生产的成年人
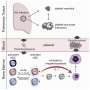
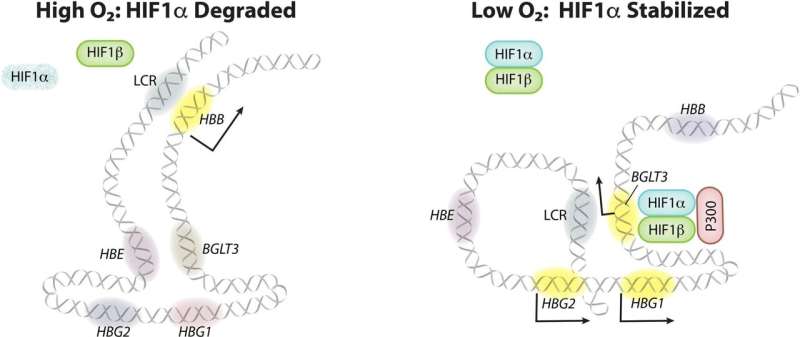
圣裘德组发现,缺氧诱导因子1 (HIF1)直接促进gamma-globin基因的转录增强住宅生产。HIF1是细胞的能力的一个重要组成部分和适应缺氧环境。在低氧条件下,HIF1积累在许多组织和激活数以百计的基因,包括红细胞的住宅。
第一作者Ruopeng冯博士,一位科学家在维斯实验室,表明药物激活的一部分细胞缺氧反应抑制的镰状红细胞来自患有镰状细胞病。的药物脯氨酸羟化酶抑制剂,导致HIF1积累,结合DNA的监管区域附近的γ球蛋白基因,激活转录产生住宅和抑制细胞“镰状”。
脯氨酸羟化酶抑制剂目前后期临床开发治疗贫血相关慢性肾脏疾病。这些药物通过稳定诱导蛋白质刺激红细胞生成素的生产,一种激素,促使红细胞生产。
“我们的发现表明,脯氨酸羟化酶抑制剂可能是有用的治疗镰状细胞病或beta-thalassemia,打开住宅生产疗效,”Weiss说。“大约有20%的成年人镰状细胞病患者出现肾功能衰竭与贫血有关。脯氨酸羟化酶抑制剂可能为这些人的双重目的,通过刺激促红细胞生成素和住宅的生产。”
将住宅的缺氧反应
诺贝尔生理学或医学奖授予2019年低氧诱导因子的发现途径。当前的研究,由维斯集团,建立一个直接连接这个低氧适应和住宅之间的表达式。这种联系解释长期临床观察期间住宅是诱导加速生产红细胞在暴露于缺氧或在某些形式的贫血,条件称为“压力红细胞生成。”
“gamma-globin作为诱导目标基因的识别支持住宅发展的概念对缺氧保护机制,”Weiss说。“血红蛋白超过50年的研究已经建立了许多一般原则在生物学和医学。令人兴奋和满足,调查血红蛋白和球蛋白基因表达继续产生新的,临床相关的发现。”
进一步探索
代码:github.com/YichaoOU/HemTools