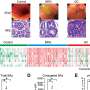
抗氧化剂启动的干细胞有望修复辐射损伤的骨
骨肿瘤的标准治疗通常是双重的:手术切除癌变部位,然后进行放射治疗,以确保所有癌细胞都被杀死。这是一种击败骨肿瘤的有效方法;然而,由于广泛的组织切断和辐射诱导的组织损伤,它常常导致巨大的骨缺损和阻碍伤口愈合。一项新研究发表在干细胞转化医学展示了阿魏酸诱导的干细胞如何修复这种骨损伤以及这是如何发生的。这项研究提供的信息可以帮助开发新的治疗辐射骨损伤的方法。
北京放射医学研究所(BIRM)的医学博士朱恒和中华人民共和国空军医疗中心的医学博士丁立是这篇论文的共同通信作者。BIRM的同事Liang Jia-Wu M.D和Pei-Lin Li M.D是共同第一作者。
“一个主要的担忧放射治疗它损害了骨骼干细胞(SSCs)的“干细胞性”,这意味着它影响了它们自我更新和分化的能力,而这些能力是骨骼干细胞的关键资产骨再生和修复,”朱博士说。“尽管如此,关于辐照后SSC茎干的变化和相关的潜在调节因素的信息很少。这限制了我们对基于scs的骨再生的理解水平。”
在寻找一种限制辐射对造血干细胞的有害影响的方法时,朱博士和他的团队对阿魏酸(FA)产生了兴趣。FA是一种强大的抗氧化剂,通常存在于水果和蔬菜中,具有很强的抗炎特性,已广泛应用于预防心血管疾病,糖尿病,癌症等。众所周知,它还能减轻辐射引起的干细胞损伤。
“考虑到SSCs在骨再生中的基础作用和FA在辐射保护中的潜在作用,我们假设FA与SSCs结合可能有效地重建辐射后的骨缺损。我们用体外细胞模型和体内动物模型探索了这一想法。此外,细胞和分子机制FA对SSCs潜在的保护作用也进行了研究,”丁博士说。
在他们的体外研究阶段,研究人员将辐照的scsc和未辐照的scsc播种到培养板上,然后添加不同浓度的FA,以确定FA对SSC增殖、分化和自我更新的潜在影响。
为探讨SSC对动物模型辐照后骨缺损的修复能力,对小鼠的后肢和下腹进行局部照射,1小时后进行骨缺损手术。未接受放射治疗的手术小鼠作为骨缺损对照组。然后将含有fa引物SSCs或单独SSCs的微低温凝胶注入辐照小鼠的骨缺损区域。在另一组辐照动物中使用相同浓度的不含SSCs的微冷冻凝胶作为对照。最后,为了研究FA对骨修复的影响,将FA溶液注入辐照骨缺损中。
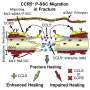
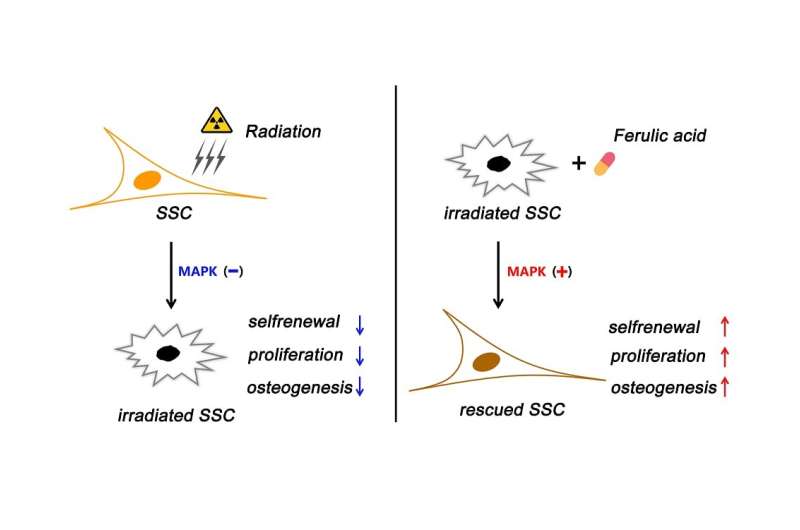
然后分别在辐射后1周、2周和3周对结果进行评估。他们发现,FA通过激活p38/MAPK和ERK/MAPK通路,显著挽救了辐射诱导的SSCs损伤。p38/MAPK和ERK/MAPK通路是细胞内的蛋白质链,负责将细胞表面受体的信号传递到DNA。因此,它们在细胞增殖、分化、发育、转化、凋亡等复杂的细胞过程中发挥着重要作用。
此外,FA显著增强了辐照骨缺损小鼠SSCs的骨修复作用。
“这项工作揭示了FA促进照射后骨骼干细胞的干细胞性的维持。该研究还将p38/MAPK和ERK/MAPK通路的激活定义为调控FA活性的分子基础机制,”梁博士说,“值得注意的是,我们的数据显示,SSC对辐射非常敏感,表现出茎干受损,这为理解骨质疏松症和辐射后骨修复受阻提供了新的信息。”
“虽然之前发表的几项研究表明FA可以增强和改善干细胞的自我更新,其活性是通过激活p38/MAPK和ERK/MAPK途径介导的,但我们的研究是第一个证明FA增强SSCs的骨修复效果,”李博士补充说。“因此,我们相信靶向SSCs有潜力作为治疗辐照骨损伤的新策略。”
“在目前的研究中,有希望的数据表明,stem细胞结合强抗氧化剂阿魏酸,增强骨骼的骨修复效果干细胞的主编安东尼·阿塔拉医学博士说干细胞转化医学维克森林再生医学研究所所长。“这些发现有一天可能会导致骨肿瘤的新治疗标准。”