新的洞察力对可以治疗亨廷顿疾病的蛋白质结构
在亨廷顿的疾病中,脑细胞中有缺陷的蛋白质聚集体,最终杀死它们。原则上,这种蛋白质聚集体可以预防热休克蛋白。然而,这些蛋白质如何与亨廷顿的疾病蛋白质相互作用。Patrick Van der Wel(格罗宁根大学)和德克萨斯大学的同事的新研究部分解决了与此类聚集蛋白结合的热休克蛋白的结构,帮助我们了解他们的工作方式。结果于2月11日发表于期刊自然通信。
热休克蛋白(HSP)由暴露于压力条件的细胞产生。HSP家族是多种多样的,并且相当多的蛋白质用作伴侣。这意味着它们以正确的方式帮助其他蛋白质折叠(或在损坏后重新折叠)。“这些蛋白质可以有助于折叠数千种不同的蛋白质。为此,他们使用具有特定绑定能力的共同伴侣,”格罗宁纳大学固态NMR光谱副教授Patrick Van der Wele解释说。
订购
一类热休克蛋白Hsp40有助于抑制类似亨廷顿氏舞蹈病(Huntington's disease)中出现的蛋白质聚集。这些Hsp40蛋白有不同的种类,其中一些会专门与含有大量重复谷氨酰胺氨基酸的聚集蛋白结合,就像在亨廷顿氏症中发现的缺陷蛋白。其中一种Hsp40蛋白叫做DnaJB8,这就是Van der Wel和他的同事研究的蛋白质。
“为了了解DNAJB8的动作,我们需要知道它看起来像什么,”Van der Wel说。然而,难以解决这种类型的蛋白质的结构。“它看起来是二聚体或低聚物,因此许多这些蛋白质单位一起工作,但它们的结构并没有真正订购,”他继续。这使得不可能使用所有需要有序结构的标准技术。
碳原子
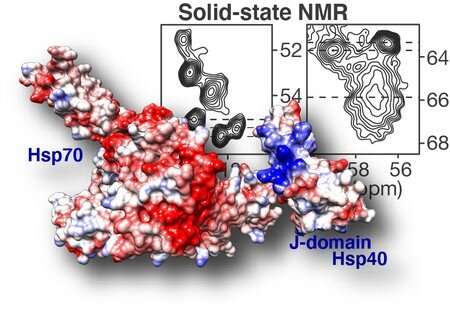
德克萨斯大学同事们提出的van der Wel,以帮助解决这个问题。van der WEL专门从事固态NMR光谱,这是一种可以测量ATOMS如何彼此连接的技术。简单来说,DNAJB8中两个连接的碳原子的NMR信号取决于它们如何与分子中的其他原子相互作用。因此,碳原子的测量光谱可以显示它们所在的氨基酸。这种信息可用于了解蛋白质的结构,即使它没有充分的命令也是如此。
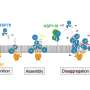
DNAJB8蛋白质由不同的域名,具有不同的功能。通过一系列实验,van der WEL能够确定哪些域在DNAJB8蛋白内粘在一起,并且可以在外面使用。实验表明,DNAJB8的所谓的“J域”能够在被卡住和可访问之间切换。这是重要的,因为DNAJB8蛋白的这一部分负责接通HSP70蛋白,这可以防止蛋白质聚集物形成。换句话说,DNAJB8似乎是一个“交换机”,它控制与HSP70的这种交互。有趣的是,发现该交换机位于DNAJB8的域中,其确切的作用先前尚不清楚。
假设
因此,我们基于结构的假设是DNAJB8是无活性,直至其结合故障蛋白质,然后它吸引HSP70,“Van der Wel说。德克萨斯大学的一系列模拟和实验证实了这一思想,并产生了这些蛋白质如何共同努力的详细模型。
DNAJB8是主要在睾丸中发现的蛋白质。然而,叫做DNAJB6的非常相似的蛋白质存在于大脑中,其中亨廷顿的疾病罢工。当它保护富含谷氨酰胺的蛋白质,似乎是这种蛋白质的可能性的可能性类似于患者脑细胞中聚集的富含谷氨酰胺的蛋白质。“可能需要更多的少年,但现在我们了解这个过程的工作原理,它可以帮助我们找到一种方法来提高DNAJB6的活动,这可以减少蛋白质导致疾病的聚集体,“梵德华州的总结道。
进一步探索









用户评论