2021年1月29日功能
SARS-CoV-2逃避我们的免疫防御系统如何?
SARS-CoV-2逃避我们的免疫防御系统如何?实际上,这是一个好问题。当SARS-CoV-2失败宿主防御,我们需要知道它,反之,当宿主防御获胜,也需要理解。第一次细胞与病毒,这是当地的先天免疫系统在受感染细胞内,弹簧必须采取行动。的时候更加分散bloodborne信号和其他系统自适应免疫反应展开,它可能是太迟了。
有几种胞质传感器在大多数细胞的核酸检测品种不应该存在。除了细胞自身的单链(ss)、积极意义(+)mRNA,存在其他胞质核酸(如双或单股DNA或RNA不同感官的)意味着要么病原体感染,从受损的线粒体mtDNA泄漏,或者总核击穿发生。在任何情况下,这些都是不祥的事件,需要解决快速细胞之前被迫推出某种autodestruct计划。
积极意义上的正常探测器病毒RNA解旋酶RIG-1,虽然解旋酶MDA5感官RNA和长dsRNA消极意义。rna与修改的核苷酸,如N-6-methyladenosine (m6A)和假尿苷核苷酸(与辉瑞疫苗)常常无法触发这些传感器。我们自己的信使rna能够逃脱通过CAP-1甲基化检测。有时候,我们的细胞使dsrna,他们的检测是避免A-to-I(肌苷腺苷)修改由腺苷脱氨酶催化(ADAR1)。
相结合的关键分子信号不同的胞质核酸防御分子之间是刺痛,即“干扰素刺激基因。”While its canonical function is to initiate the cGAS–STING pathway in response to cytosolic dsDNA, it is now known to participate in downstream RNA detection pathways, as well. It should not be surprising that sensing pathogenic patterns of cytosolic nucleic acids is a fundamental and conserved feature of most forms of life. In a recent paper in生化科学趋势作者塞缪尔一起支持件的进化起源刺信号并探讨它作为治疗目标。的劳动成果有广泛的影响细胞过程涉及炎症和自噬,扩展了我们理解细胞防御病毒感染和多种癌症的成因。
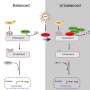
cGAS-STING的工作方式是,DNA识别后,注册会计师(循环GMP-AMP合成酶)二聚和刺激形成cyclic-GMP-AMP (cGAMP)。这种构造然后结合并激活刺痛。反过来,刺磷酸化的转录因子通过TBK1 IRF3,然后进入细胞核转录促进炎症像IFN-β干扰素。我问撒母耳为什么自然普遍决定合成循环二核苷酸胞质核酸的响应。具体来说,核酸是否被分解为单个核苷酸(deoxynucleotides),转化为国家结核控制规划,然后信号cGAMP用作基质;是否可能会有大量的嘌呤国家结核控制规划中已有的基质细胞。虽然这个问题还没有解决,至少在他的知识,可能会有一些相似之处与常见的循环nucletides代细胞外甚至线粒体g蛋白信号转导。
得到一个真正的感觉刺痛是什么,有必要回头看,试图揭示成立的目的。刺蛋白质序列的分析表明,其干扰素信号活动,由其c端尾部区域,是一个相对最近的加法。其主要守恒的作用似乎是广义诱导细胞自噬,通常针对胞质dsDNA。在更原始的微生物如大肠杆菌和诉霍乱、刺痛的伙伴,排气口,防止相邻细菌噬菌体感染的传播通过激活磷脂酶A2。这导致孔隙形成的细菌内膜并最终死亡。
它是什么,刺是一个重要的目标,许多病毒灭活为了增加他们的传染性。例如,Zika病毒、登革热病毒、西尼罗河病毒、乙型脑炎病毒和丙型肝炎都有块STING-mediated信号的方法。一些蛋白酶可以分裂刺痛或注册会计师,和其他人可以抑制STING-TBK1交互,这将抑制干扰素轴但备用NF-KB手臂的响应。作为一个包裹,积极的意义上,单链RNA病毒,SARS-CoV-2可能引起胞质核酸传感器的注意像刺在生命周期的不同时间点。其骨干类似于我们的信使rna,因此立即由宿主细胞翻译。消极意义上讲病毒RNA信使RNA的补充,因此必须转化为积极意义RNA的RNA聚合酶在翻译之前。其dsRNA复制的中间形式也可能是一个目标,尽管病毒经常隐藏背后的双层光学膜。
SARS-CoV-2本身诱发多种延迟细胞损伤,导致释放mtDNA dsDNA和其他类型。非典膜(M)蛋白被发现抑制我和III型干扰素生产针对RIG-1和MDA5通过抑制的痛。通常情况下,激活RIG-1从事线粒体抗病毒信号蛋白(小牛),因此复杂的修改与K63-polyubiquitin链。这些小牛然后迅速形成prion-like聚集,然后连续转换其他线粒体外膜上的小牛。尽管这个过程的全面影响尚未理解,SARS-Co-V-2插图很重要的特性,我们很快就和应用在我们的斗争。
©2021科学欧宝app网彩X网络