深入研究杜氏肌萎缩症的差异
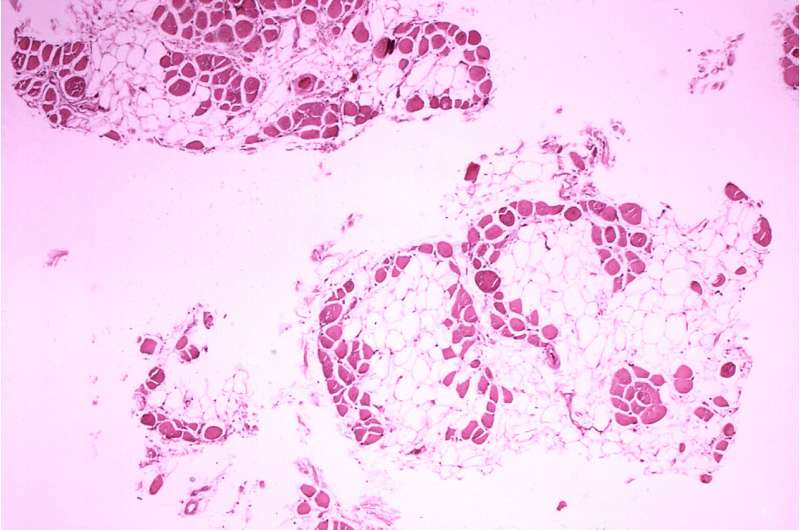
德克萨斯大学西南分校的一个研究小组对小鼠骨骼肌的基因活动进行了分类,并将健康的动物与那些携带导致人类杜氏肌萎缩症(DMD)基因突变的动物进行了比较。研究结果最近发表在pnas.,可能会导致这种毁灭性退化性疾病的新疗法,并深入了解影响肌肉发育的因素。
了解活动的基因可以脱落在体内影响不同组织的病理学上。然而,朗达巴塞尔 - 拜访,博士,在UTSW的分子生物学教授,学习骨骼肌由于其他组织类型的关键差异,这是一个挑战;而不是含有控制基因活性的单个核,而不是骨骼肌肉纤维可以包含数百个核。并且它未知在所有这些细胞核中激活哪种基因,使得尚不清楚基因表达在受DMD影响的健康骨骼肌组织和组织之间的不同之处。
回答这些问题,埃里克奥尔森,博士,博士,博士,博士 - 拜特,兼胫塞尔和他们的同事从胫骨上孤立的组织,一只小鼠的肌肉,类似于胫骨的人类。他们从健康动物中和DMD的小鼠模型中取出了这些样本,即它们使用基因编辑技术产生的突变,以引入通常导致人们DMD的突变。然后,研究人员从两组肌肉纤维中分离出两组动物的肌肉组织,科学家基于类似的基因谱确定14种核。这些核似乎基于其主要的占主导地位执行不同的工作基因活性,例如维持成熟肌肉,与神经元或肌腱一起联络,或再生新的肌肉纤维。研究人员还确定了其他类型细胞的细胞核,例如平滑肌细胞如内皮细胞、产生脂肪或结缔组织的细胞,以及称为巨噬细胞的免疫细胞。
当研究人员比较健康和DMD小鼠的这14个不同的细胞核时,他们发现了显著的差异。例如,与健康的动物相比,患有DMD的动物的成熟肌肉核明显更少。相反,巨噬细胞明显增多,这反映了DMD肌肉中的炎症,以及健康组织中根本不存在的一类再生细胞。参与与神经连接的核细胞和肌腱有最差异基因表达这表明在所有类型的细胞核中,它们受DMD的影响最大。
此外,几乎所有从DMD动物中分离出来的肌肉核在泛素途径(标记降解蛋白的途径)上的基因活性都增加了,以及在凋亡或细胞死亡中起作用的基因的更高活化,这反映了DMD特征的肌肉降解。
Bassel-douby注意到该研究有几个关键限制:例如,所使用的技术没有揭示肌肉细胞核位于肌肉组织内的位置,这可能会赋予核如何相互通信的有价值的线索并影响基因活动。如果修补导致DMD可能将基因激活恢复到正常的基因突变,也仍然未知。她和她的同事计划在未来的研究中调查这些问题。
通过制定更好地理解肌肉纤维如何在健康和患病中运作组织她补充说,研究人员最终可以学会操纵基因活动以获得最佳水平。作为一种更直接的目标,鉴定DMD患者的差异可能导致新的治疗目标。
“鉴定这些中的特定基因活动核可以为我们提供以前被忽视的治疗方法的新思路,”Bassel-Duby说。“最终,我们可以找到防止这些患者肌肉退化的方法,并提高他们的生活质量。”
“我们的研究为Duchenne肌营养不良的分子底划处于前所未有的分辨率水平,并突出了这种疾病中的中央角色的基因和信号通路的集合,”添加了Olson。“这项工作开辟了通过药理或遗传干预改善这种疾病严重病理学后果的新方法。”
进一步探索











用户评论