研究阐明了为什么视网膜神经节细胞易患青光眼
数百万青光眼患者有一天可能从今天发表的一项研究中受益干细胞在该研究中,“培养皿中的疾病”干细胞模型被用于检查青光眼中导致视网膜神经节细胞(RGCs)退化、导致视力丧失的机制。这项研究提供的知识可能导致新的治疗方法,用于治疗这一全球失明的主要原因。
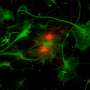
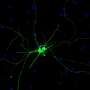
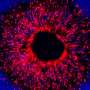
rgc是一组神经细胞视网膜位于视网膜上,将图像传送到大脑,使你能看见东西。青光眼攻击这些细胞,一旦它们死亡,它们就无法再生。然而,为什么和如何青光眼导致rgc退化的原因是一个谜。
这种疾病的干细胞模型可能会揭示这一点。在过去的十年中,诱导多能干细胞(iPSC)技术在模拟青光眼方面取得了重大进展。这包括从iPSCs中生成人类rgc,这导致了原发性开角型青光眼(POAG)(青光眼最常见的形式)的疾病模型的开发,以及一个视神经模型,该模型证明了mTOR信号在化学轴突切开术后hRGC轴突再生中的支持作用。
内布拉斯加大学医学中心的Iqbal Ahmad博士说:“然而,这两种模型都可以通过描述对照和疾病特异性rgc的发展轨迹来改进。”他和他的UNMC同事Pooja Teotia博士和孟Niu博士进行了一项研究干细胞.
Ahmad博士继续说:“这一特征包括hrgc在正常发育时间和阶段的生成,其中包含不同亚型的补充,据此可以评估疾病模型中RGC异常的发育方面。关于不同RGC亚型的信息不仅从功能角度很重要,而且对于理解青光眼退行性变的潜在机制也很重要,因为有新证据表明,RGC的敏感性和耐药性与亚型有关。”
在开发他们的模型时,研究人员使用了从正常(对照)和SIX6风险等位基因iPS细胞中产生的人类rgc的单细胞转录组分析。(之前的研究已经发现POAG和SIX6基因之间存在显著的关联,SIX6基因在眼部发育中起着重要作用。)
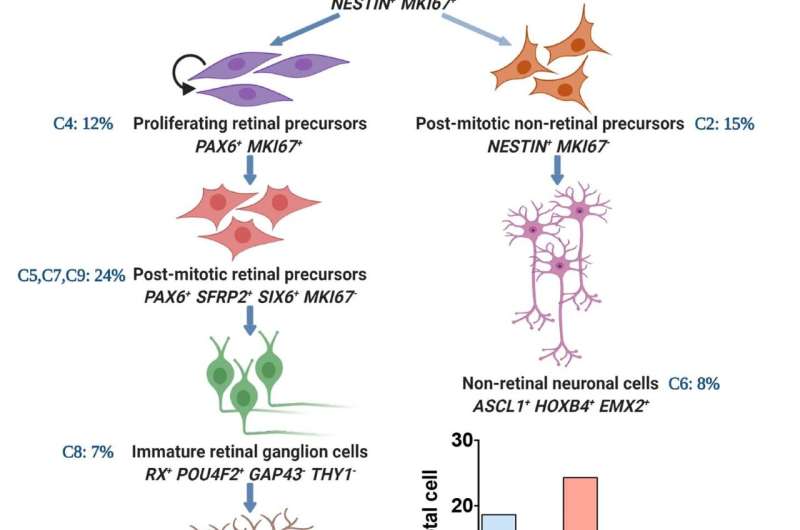
他们观察到发育轨迹,从神经开始干细胞对RGCs, SIX6风险等位基因与对照组RGCs差异无显著性。
“然而,”艾哈迈德博士说,“我们观察到,与对照组相比,SIX6风险等位基因rgc的分化在视网膜祖细胞阶段停滞,使它们保持不成熟和亚型组成不足。这可能是由于调控失调的mTOR和Notch信号通路在RGC的发展中发挥重要作用。此外,”他补充说,“与对照组相比,SIX6风险等位基因RGC表达较少对应于优先抵抗变性的RGC亚型的基因。
他总结说:“SIX6风险等位基因rgc的不成熟表型与抗退行性变亚型的代表性不足,可能使它们容易发生青光眼退行性变。”
“这项研究证明了单细胞测序方法的力量,为POAG病理学在细胞和分子水平上这对于制定新的治疗方法是必要的”,《柳叶刀》杂志主编Jan Nolta博士说干细胞.“这真的是了不起的,在13年前,直到患者特异性iPSC疾病建模的概念发明之前,我们无法想象的事情是可行的。这是向前迈出的极好的一步,我们将看到这种现象成为疾病表型和药物发现的日常现实。”