注入病毒输送基因消音器块ALS退化,节省了运动机能

写在自然医学,一个国际研究小组由加州大学圣地亚哥医学院的研究人员描述了一种新的方式来有效地交付一个基因沉默载体的成年人肌萎缩性脊髓侧索硬化症(ALS)小鼠,导致长期抑制的退行性运动神经元疾病如果治疗向量是疾病发作之前,和阻塞疾病进展的成年动物如果当开始治疗,症状已经出现了。
研究结果发表在2019年12月23日,在线杂志自然医学。马丁·马沙拉白葡萄酒,医学博士,教授在加州大学圣地亚哥分校医学院的麻醉学和桑福德财团的成员对于再生医学,是这项研究的资深作者。
ALS是一种神经退行性疾病影响大脑和神经细胞脊髓。运动神经元是专门负责沟通运动伤害,随后,渐进式肌肉不受控制影响的能力说话,吃饭,运动和呼吸。每年有超过5000美国人被诊断出患有肌萎缩性侧索硬化症,目前估计有30000人患有这种疾病。虽然有治疗ALS症状,目前还没有治疗方法。大多数病人屈服于疾病诊断后2到5年。
有两种类型的肌萎缩性侧索硬化症,零星和家庭。零星的最常见,占90 - 95%的病例。它可能会影响任何人。家族性肌萎缩性侧索硬化症占5 - 10%的病例在美国,是遗传的。先前的研究表明,至少有200突变的基因SOD1与肌萎缩性侧索硬化症。
的SOD1基因通常用于提供指示酶超氧化物歧化酶,广泛用于分解过氧化物radicals-toxic氧分子的副产品正常细胞的过程。先前的研究已经表明SOD1基因突变可能导致无效的清除超氧化物自由基或创建其他毒性造成运动神经元细胞死亡,从而导致肌萎缩性侧索硬化症。
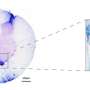
新方法是注射shRNA-an人工RNA分子能够压制或关闭目标基因传递到细胞通过一种无害的腺相关病毒。在新的研究中,单一注射shRNA-carrying病毒被放置在两个网站在成年小鼠的脊髓表达的ALS-causing突变SOD1基因,疾病发作之前或者当动物开始出现症状。
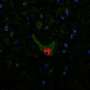
早期的努力在其他地方引入涉及沉默向量静脉注射或脑脊液在早期症状的老鼠,但疾病进展,而推迟,继续和老鼠不久就死了。在新的研究中,一个单纯注入(pia以下交付,微妙的内心膜包围大脑和脊髓)明显减轻神经退化pre-symptomatic老鼠,它显示正常神经功能没有可检测疾病发作。和几乎完全保护的功能作用运动神经元和其他细胞,包括神经元之间的连接和肌肉纤维。
在成年老鼠已经显示ALS-like症状,注射进一步有效阻止疾病进展和运动神经元变性。
在这两种方法中,老鼠生活没有影响负面影响长度的研究。
“目前,这个治疗方法提供了有史以来最有效的疗法证明突变的小鼠模型SOD1资深作者马丁说:“基因ALS马沙拉白葡萄酒,医学博士,教授在加州大学圣地亚哥分校医学院的麻醉学。
“此外,有效的脊髓交付AAV9向量在成年动物表明这个新的交付方法可能有效的治疗其他遗传形式的肌萎缩性侧索硬化症或其他需要脊髓实质的脊髓神经退行性疾病的治疗基因或突变基因沉默机制,比如在C9orf72 mutation-linked ALS基因或在某些形式的溶酶体储存疾病。”
研究小组还测试了成年的猪注射的方法,其脊髓尺寸类似于人类,安全性和有效性。使用注射设备开发用于成年人,他们发现过程可以可靠地执行,无手术并发症。
马沙拉白葡萄酒表示下一步涉及额外的安全性研究大型动物模型来确定最优,安全剂量治疗的向量。“虽然没有检测到治疗相关副作用被认为在小鼠治疗后一年多,安全的定义更类似于人类的大的动物物种是一个关键的步骤,推进这一治疗方法对临床测试。”