研究发现了导致肿瘤的潜在目标

辛辛那提大学(University of Cincinnati)的研究人员发现了针对激活某种蛋白质复合物所涉及的分子过程的其他方法,从而可能开发出治疗导致肿瘤的疾病的新疗法。
这些发现发表在11月11日的杂志上自然的新陈代谢。
“结节性硬化症复杂或TSC,是一种遗传性疾病,肿瘤在许多不同的器官,包括大脑,影响多达50000人,每年在美国“Chenran Wang博士说共同通讯,论文的主要作者和加州大学癌症生物学系助理教授。“在新生儿和成人中,TSC还会导致癫痫和自闭症等问题,从而影响大脑。在这种情况下,被称为Tsc1或Tsc2的基因突变导致其肿瘤抑制功能的丧失,反过来,导致mTORC1的过度激活及其功能异常,导致了TSC的多种症状。”
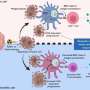
被称为“主调节器”细胞, mTORC1参与引起大多数细胞生长活性;然而,它并不促进自噬-当一个电池基本上吃掉自己时的一种调节方法,也是电池内部燃料产生的一种有效方式。
在这项研究中,科学家发现没有Tsc1的细胞具有更高的自噬活性;然后他们创造了一个“双击倒”动物模型-一种在发育中的神经系统和成年神经干细胞中均不存在Tsc1和一种必需的自噬蛋白FIP200的模型。
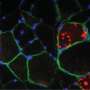
“使用这种独特的模型,我们发现了自噬作为保持mTORC1活性高的一种方式的基本功能,并显示了没有Tsc1的神经干细胞的异常发育,”王补充道。
研究人员观察了自噬的分子和代谢机制,这些机制参与维持mTORC1的高活性,并发现它需要激活能量存储,即没有Tsc的细胞中的脂滴。
“脂滴的自噬分解提供脂肪酸作为能量来源,以维持tsc1缺陷神经干细胞的能量生产,”王说。“我们还使用了药理学方法来靶向自噬并阻断脂肪酸用来治疗缺陷,在这些模型中模拟人类TSC症状。”
该研究的共同通讯作者关俊林说,这些结果是扩大这种疾病形成的知识的关键,以及它如何能够靶向治疗分子水平上。
“我们现在对TSC基因突变和过度活跃的mTORC1引起的涉及TSC的信号通路和代谢改变有了更多的了解,”加州大学的Francis Brunning捐赠主席和癌症生物学教授说。“这将有助于开发治疗这种毁灭性疾病患者的新治疗理念。”
进一步探索














用户评论