一流的dna编码单克隆抗体疗法迅速进入临床
Wistar研究所与合作伙伴Penn Medicine和Inovio Pharmaceuticals, Inc.宣布,FDA已批准启动首个人体临床试验,调查用于预防寨卡病毒感染的新型合成dna编码单克隆抗体(DMAb)治疗技术的安全性和耐受性。
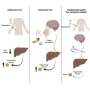
DMAb治疗技术不同于所有已知的常规治疗抗体,因为DMAb是在人体内制造的,而不是制造工厂。患者接受DNA指令,使他们的身体具备必要的工具,以制造他们自己的高度特异性抗体,对抗致病目标,如细菌、病毒感染的细胞和病毒癌症细胞.
David B. Weiner博士,执行副总裁,疫苗中心主任,Wistar癌症研究W.W. Smith慈善信托教授,一直领导DMAb技术的研究和开发。
“DMAb技术正在改变我们所知道的临床故事。在过去的几年里,我们进行了详细的临床前研究,开发了这个新平台,并证明了使用CELLECTRA传递系统在体内生产单克隆抗体。”Weiner说。“这种方法代表了对传统单克隆抗体方法的重大进步的潜力,并可能拓宽治疗策略,为基于抗体的治疗的好处开辟新的患者市场疾病预防或治疗。”
2016年,比尔和梅林达·盖茨基金会向Wistar研究所提供资金,将DMAb技术从原型转化为根除一种新出现的传染病的临床候选。
在短短两年内,寨卡单克隆抗体的一期临床试验现在正在招募参与者。该试验将由宾夕法尼亚大学佩雷尔曼医学院传染病学教授Pablo Tebas博士领导。这是一项单中心、开放标签、剂量递增试验,将招募多达24名健康志愿者,他们将接受最多4剂Inovio疫苗/产品INO-A002。
“这是一项全新的技术,可以改变我们将抗体作为治疗剂的方式,并有可能被快速追踪临床试验.虽然还有一些问题需要回答,但这不仅对寨卡病毒有用,对其他新出现的感染也有用。”特巴斯说。
“虽然这项试验针对的是寨卡病毒感染,但我们将从这项研究中获得重要数据,以开发更广泛的DMAb靶向项目传染病Inovio制药公司总裁兼首席执行官J. Joseph Kim博士说。“我们的共同目标是开发这种新的、独特的单克隆抗体方法技术这将允许一个新的高影响力DMAb产品管道,可以通过企业合作伙伴关系、外部资金和合作来开发。”