诊断卵巢癌的新血液测试
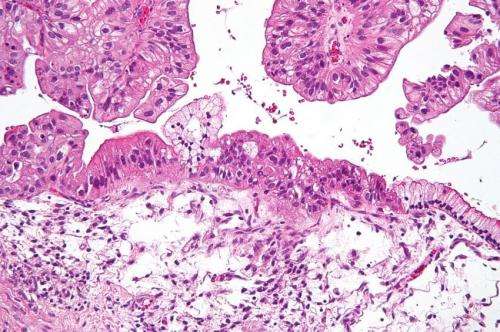
布里格姆妇女医院(Brigham and Women's Hospital)和丹娜-法伯癌症研究所(Dana-Farber Cancer Institute)的研究人员正在利用人工智能的力量开发一种新技术,以早期和准确地检测卵巢癌。该团队已经确定了一个循环的microrna网络——小的、非编码的遗传物质片段——与卵巢癌风险相关,可以从血液样本中检测到。他们的研究结果发表在eLife.
大多数女性在卵巢癌晚期被诊断为卵巢癌,此时只有大约四分之一的患者能存活至少5年。但对于在早期偶然发现癌症的女性,存活率要高得多。目前,没有fda批准的卵巢癌筛查技术存在,这使得在具有卵巢癌遗传易感性的女性或普通人群中早期诊断该疾病具有挑战性。
卵巢癌是相对罕见的其他良性妇科疾病,如卵巢囊肿.但早期检测,如超声波或CA125蛋白检测,对卵巢癌有很高的假阳性率。临床试验发现,当这些测试被用于检测早期卵巢癌时,它们对生存率没有显著影响。Dana-Farber和BWH团队寻求一种更敏感、更特异的工具来检测早期疾病的真实病例。
该团队研究了一组名为microRNAs的分子,这是基因组的非编码区域,有助于控制基因在何时何地被激活。
“microrna是基因组的文案编辑:在基因转录成蛋白质之前,它们修改信息,给基因组添加校对注释,”BWH妇产科的首席作者Kevin Elias医学博士说。
“该项目体现了DFCI和BWH这两个研究所的协同作用,以及临床医生与实验室科学家密切合作的力量。我的实验室一直致力于microrna十年,当凯文来到我们与患者样本,这是一个显而易见的启动这个项目”Chowdhury说,资深作者Dipanjan博士,部门的首席辐射和基因组的稳定在DFCI放射肿瘤学部门。
在实验室里,伊莱亚斯和乔杜里以及他们的同事确定了这一点卵巢癌细胞和正常细胞有不同的microRNA谱。与遗传密码的其他部分不同,microrna在血液中循环,这使得从血清样本中测量其水平成为可能。该团队对135名女性(术前或化疗前)血液样本中的microRNA进行了测序,以创建一个“训练集”,用它训练计算机程序寻找卵巢癌、良性肿瘤、非侵入性肿瘤和健康组织之间的microRNA差异。使用这种机器学习方法,该团队可以利用大量的microRNA数据,开发不同的预测模型。最准确区分卵巢癌与良性组织的模型是神经网络模型,它反映了microrna之间复杂的相互作用。
“当我们训练计算机寻找最佳的microRNA模型时,这有点像在夜空中识别星座。一开始,只有很多亮点,但一旦你发现了一种模式,无论你在世界上什么地方,你都能找到它。”
研究小组随后在一个由44名女性组成的独立小组中测试了这个测序模型,以确定该模型的准确性测试.一旦模型的准确性得到确认,该团队将该模型部署在多个患者样本集上,总共使用859例患者样本来测量模型的敏感性和特异性。这项新技术在预测卵巢癌方面比超声检测要好得多。然而使用超声波检测不到5%的异常结果会是卵巢癌,而使用microRNA检测几乎100%的异常结果实际上代表卵巢癌。最后,该小组将他们的最终模型付诸实践,使用microRNA诊断测试来预测在波兰罗兹接受外科治疗的51名患者的诊断。在这一人群中,91.3%的异常检测结果是卵巢癌病例——假阳性率非常低。阴性测试结果可靠地预测了80%的情况下没有癌症,这与巴氏涂片测试的准确性相当。
“关键是,这种检测不太可能误诊卵巢癌,并且在没有恶性肿瘤的情况下给出阳性信号。这是有效诊断测试的标志。
该团队还寻找了区分微rna的生物学相关性的证据。他们发现,在手术前后采集的血液样本中,这些microRNA的数量发生了变化,这表明癌变组织被移除后,microRNA信号减弱。他们还采集了实际患者的样本,并对癌细胞中的microrna进行了成像,表明血清信号来自于癌细胞组织。
为了将诊断工具从实验室转移到临床,研究团队将需要验证microRNA标记如何随着时间的推移而改变卵巢风险癌症增加。要做到这一点,他们需要使用前瞻性收集的纵向样本,长期跟踪女性。他们特别感兴趣的是确定该工具是否对高危妇女有用卵巢癌以及普通大众。
进一步探索








用户评论