FDA批准脐带血干细胞产品血液癌症患者
美国食品和药物管理局批准Omisirge (omidubicel-onlv)大幅修改同种异体绳blood-based细胞疗法,以减少感染的风险血癌患者骨髓后治疗,如放疗或化疗。
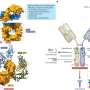
Omisirge管理作为一个单一的,针对病人的静脉注射剂量血液癌症患者中性粒细胞≥12年加速复苏。治疗是由人类从脐带血捐赠干细胞与烟酰胺处理和培养。
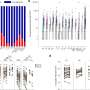
批准是基于数据从一个随机、多中心研究比较移植Omisirge脐带血移植,患者在125年血癌(年龄、12和65年)。患者随机分配到Omisirge, 87%达到中性粒细胞恢复治疗后12天的中位数和83%的参与者随机分配接受脐带血移植(中性粒细胞恢复平均22天)。在100天内的移植,细菌或真菌感染被认为在39%的那些收到的接收Omisirge和60%脐带血。
“今天的批准是一个重要的促进细胞疗法治疗患者的血液癌症,”彼得痕迹,医学博士博士,FDA生物制品评价和研究中心主任,在一份声明中说。“加速人体白细胞的回归可以减少感染严重或压倒性的可能性与干细胞移植有关。”
版权©2023每日健康。保留所有权利。