增强对癌症的免疫反应
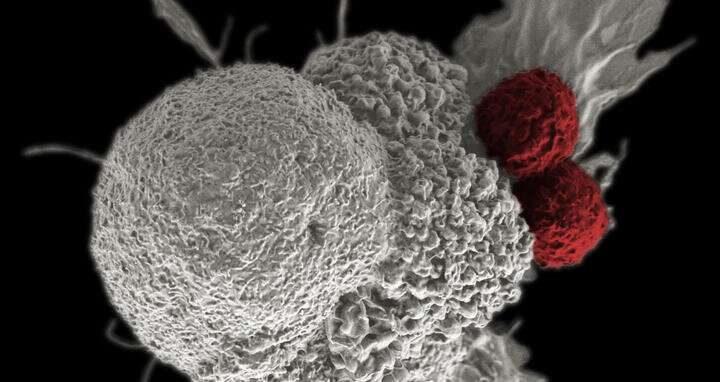
T细胞通常在消灭病变细胞方面表现出色,但在消灭肿瘤细胞方面似乎无能为力。在江森自控的洞察力在美国,由Armin Rehm和Uta Höpken领导的MDC团队描述了抑制这种免疫功能的因素,以及他们如何释放刹车并增强对癌症的免疫反应。
T细胞是免疫系统的特警队。它们的工作是不断巡视血液、淋巴系统、组织和器官。如果它们遇到被病原体污染或破坏的细胞,它们就会消灭它们。它们还能识别并摧毁癌细胞。但问题是肿瘤细胞想办法逃离这道防线。世界各地的研究人员都在努力防止这些规避策略,并利用T细胞进行针对癌症的靶向免疫治疗。
柏林Helmholtz协会(MDC)分子医学Max Delbrück中心的Armin Rehm博士和Uta博士Höpken领导的实验室现在已经确定了肿瘤细胞用来躲避人体免疫反应的机制。
“在许多情况下,肿瘤细胞特别频繁地读取EBAG9基因。然后这些细胞产生一种保护它们的蛋白质。但是EBAG9也会影响免疫系统的细胞,因为T细胞也会产生EBAG9。在T细胞中,EBAG9抑制酶的分泌,这种酶作为毒药杀死肿瘤细胞,”Rehm说。
写日记江森自控的洞察力“我们关闭了EBAG9基因,”在Rehm研究小组工作的联合第一作者Anthea Wirges博士说。“这意味着我们可以阻止T细胞产生EBAG9,并长期加强对癌症的免疫反应。”
EBAG9解除了免疫细胞的武装
科学家们已经知道癌细胞可以智取免疫细胞.这一知识导致了检查点抑制剂的发展,这是一种已经在临床使用的免疫疗法。检查点抑制剂使得癌细胞很难欺骗T细胞,让T细胞认为它们是无害的。“但是EBAG9为癌细胞提供了另一道对抗免疫系统的防线,”Rehm说。“它解除了免疫细胞的武装,阻止它们分泌伤害人体的物质癌症细胞."
Rehm和Höpken一直怀疑EBAG9抑制T细胞。2009年,雷姆的团队开发了一种小鼠模型研究人员关闭了EBAG9基因。“小鼠的免疫系统在没有EBAG9的情况下工作得更好,它们能够更有效地对抗感染,”Rehm说。Höpken的团队随后将无ebag9的小鼠与另一种自发发生白血病的转基因小鼠模型进行杂交。Höpken说:“我们在很长一段时间内观察了这些经过双重修饰的老鼠。”“它们的肿瘤发展比携带EBAG9的小鼠慢得多。”
癌症和感染会引发不同的免疫反应
Wirges用单细胞RNA测序和生物信息学方法检查了EBAG9基因对T细胞的影响。除了证实EBAG9抑制T细胞反应外,数据还表明,对癌症的免疫反应不同于由感染引发的免疫反应。
“关于免疫系统如何形成‘记忆’的知识来自感染模型。它不能以1:1的比例转移到肿瘤,”Rehm说。T细胞通过其表面的信号分子来识别患病或感染的细胞。当它们检测到这些有害结构时,就会分化成细胞毒性T细胞和记忆性T细胞。
细胞毒性T细胞分泌蛋白质,在靶细胞的细胞膜上穿孔,这样它们就能穿透靶细胞,通过中毒杀死靶细胞。感染的组织也会产生炎症信号分子例如细胞因子,它会召唤更多的T细胞,并使它们成熟为记忆T细胞。记忆单元记录免疫反应这样T细胞每次检测到疾病时,免疫系统就不必从头开始了。
他们的想法是:制造没有免疫制动的CAR - T细胞
肿瘤在早期不会引起炎症。此前,科学家们认为这是因为T细胞不能很好地识别肿瘤细胞。Höpken说:“因为肿瘤细胞是由身体产生的,所以肿瘤细胞的表面分子很少可以被识别为外源细胞。”但似乎这些微小的差异足以让T细胞发现肿瘤细胞:当研究人员关闭EBAG9时,反应是惊人的。“未受抑制的T细胞非常早地、非常彻底地消除肿瘤细胞,”Rehm指出。这也创造了对肿瘤细胞的持久保护。“最初的T细胞反应越强,随后的T细胞记忆就越好,”Rehm说。
“基于这些发现,我们现在想开发不含EBAG9的CAR - T细胞作为白血病的免疫疗法,”Wirges说。汽车代表嵌合抗原受体这是一种人工受体,可以检测肿瘤细胞,并与患者自身的T细胞相结合。当病人接受CAR - t细胞输注时,他们的身体就会有能力对抗癌症的细胞。MDC的研究人员希望CAR - T细胞在没有EBAG9的情况下更有效。尽管这些细胞进入临床试验阶段还需要一段时间,但等待是值得的:“我们不只是希望这种疗法能对白血病和淋巴瘤产生更有效的治疗效果。我们希望它能治愈它们,”Rehm说。
进一步探索