生物标志物发现可能是针对致命形式的脑癌的药物靶标
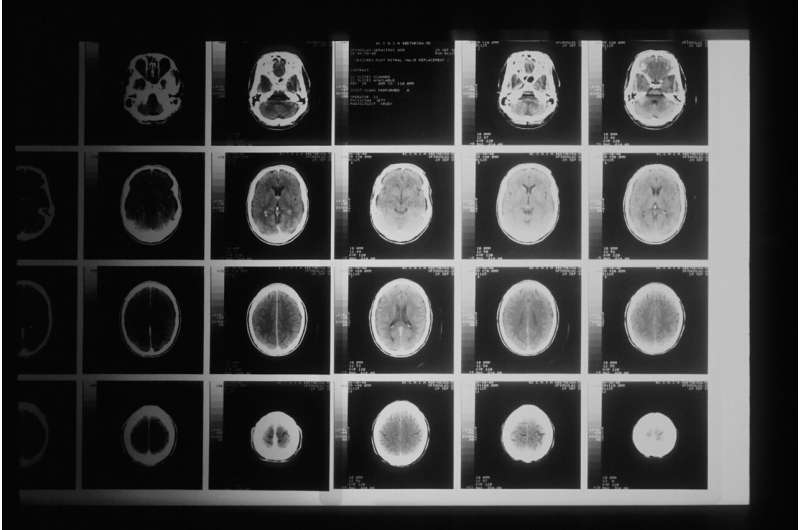
乔治敦伦巴第综合癌症中心的研究人员已经鉴定出可能是治疗胶质母细胞瘤脑肿瘤的新型药物的生物标志物,从而为高度致命的癌症提供了希望。
目前,该药物通常用于治疗胶质母细胞瘤,替莫唑胺具有独特的能力跨越血/脑屏障以攻击肿瘤,但耐药性迅速发展,许多患者在诊断后一年超过一年的生存。这一新发现提供了早期证据,表明针对特定更改可能会有好处癌细胞一旦患者的肿瘤变得对替莫唑胺具有抗性,较新的药物就会具有抗性。
该发现出现在2022年6月22日科学进步。
“作为一个领域,我们一直在努力应对替莫唑胺的短期有效性,因为随后在胶质母细胞瘤临床试验中对其他癌症进行了成功使用的许多药物令人失望。了解我们如何针对有助于药物抗药性胶质母细胞瘤生存的功能的知识足以生存。“我们重点介绍了替莫唑胺如何损害DNA以帮助辐射治疗更好地工作的细节。我们的团队发现,抗替莫唑胺耐药的胶质母细胞瘤依赖于一种称为CLK2的蛋白质,并且抑制CLK2活性会导致广泛的混乱,导致癌细胞死亡,导致癌细胞死亡。”
研究人员确定的目标是DNA和RNA的关键结构成分的改变,特别是在鸟嘌呤中,鸟嘌呤是构成DNA的四个碱基之一。对鸟嘌呤的修改最终会对CLK2产生影响,这与肿瘤的侵略性有关。除了确定脆弱的修饰外,研究人员还能够鉴定出有助于稳定RNA的药物,并可能降低或阻止通常发展为替莫唑胺的抗性。
诊断和中位生存期后,只有大约5%的被诊断患有胶质母细胞瘤的患者活了五年多了。自1970年代中期以来,生存率并没有太大变化。自2005年以来,Temozolomide(Temodar)与手术和辐射结合使用。
Temozolomide的靶向鸟嘌呤还会影响调节致癌基因关键基因的结构。如果这些癌症- 可能会关闭称为致癌基因的基因,该药物的活性可能更长。这些知识中的一些知识是从神经发生疾病,肌萎缩性侧索硬化症(ALS)的研究中收集的,通常称为Lou Gehrig病。ALS具有与胶质母细胞瘤相似的某些特征,因此它们还可能为胶质母细胞瘤治疗的新策略提供信息。
“一些机制神经退行性疾病似乎与胶质母细胞瘤的替莫唑胺耐药性有关。这项研究开始时,泰克(Tiek)是里金斯(Riggins)实验室的博士学位学生。看看你是否正确。”
研究人员现在正在对小动物模型进行研究,他们将测试新颖的CLK2抑制剂是否可以有效地进入大脑并收缩替莫唑胺- 抗性胶质母细胞瘤。“我们还在调查其他是否抗癌药攻击鸟嘌呤,通常在三阴性乳腺癌和结直肠癌,例如,以类似的方式改变RNA结构,这可以使CLK2抑制在这些癌症的复发性,耐药形式中更有效。” Riggins总结道。
进一步探索