早期的hiv - 1感染背后调查机制
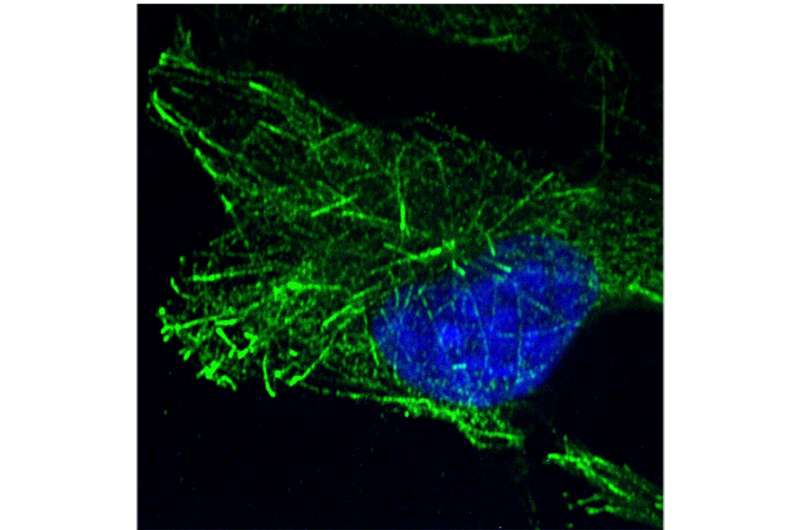
西北医学调查人员发现,抑制微管蛋白早期感染艾滋病病毒1型(HIV - 1),根据研究结果发表在美国国家科学院院刊》上。
萨耶达·摩根·Naghavi博士Microbiology-Immunology教授的西北大学的罗伯特·h·劳瑞综合癌症研究中心,该研究的资深作者。
许多病毒需要dynein-dynactin motor-adaptor复杂,负责的胞内运输货物沿着微管在细胞的细胞骨架到达细胞核。病毒利用这个复杂的到达细胞核和启动感染。
许多病毒直接绑定到微管马达蛋白在细胞内旅行,但是以前的工作表明,hiv - 1使用不同的细胞机制间接参与汽车适配器。此外,与许多病毒,hiv - 1不需要蛋白质dynactin-1 (DCTN1)——核心组件dynactin货物适配器dynein-and这个现象的重要性仍然未知,根据作者。
通过分析细胞感染hiv - 1, Naghavi和他的同事们发现DCTN1能抑制hiv - 1感染早期通过干扰病毒核心的能力,或衣壳壳周围的基因组病毒与重要的代数余子式(非蛋白物质)在宿主细胞内。
具体来说,DCTN1争夺绑定到hiv - 1颗粒细胞质蛋白质链接器170 (CLIP170),一个微管左端的跟踪蛋白质(+小费),研究人员先前显示调节稳定性的病毒进入细胞后核心。
在当前的研究中,他们发现DCTN1影响感染没有dynactin复杂的组件,而是作为一个+提示绑定和隔离CLIP170从传入的hiv - 1相互作用粒子。
“这DCTN1的负面作用在调节+提示功能dynactin复杂之外提供了一个理由为什么hiv - 1可能已经远离DCTN1意味着参与动力蛋白,“Naghavi说。“我们的发现不仅提供了一个解释为什么hiv - 1已经远离使用DCTN1作为汽车适配器,但也揭示了机械的见解更广泛的功能贡献+控制hiv - 1的建议感染。"
根据Naghavi,发现可以提高小说治疗hiv - 1治疗策略的发展,当前针对微管的药物细胞,比如目前用于化疗,是有毒的。
“更精致的药物目标高度专业化微管监管机构可能会是一个有吸引力的方法开发新的,无毒的治疗策略来治疗hiv - 1,”Naghavi说。
更多信息:Shanmugapriya Shanmugapriya et al, Dynactin 1负调节隔离主机代数余子式CLIP170 hiv - 1感染,美国国家科学院院刊》上(2021)。DOI: 10.1073 / pnas.2102884118