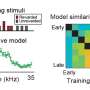
钠离子通道的分子组成的变化可能使药物疗效
精密医学研究每个人的独特的基因构成,生活方式和环境在考虑治疗疾病和疾病。圣路易斯华盛顿大学的一个研究小组正在采取措施向发展中精密医学患者不规则心跳通过研究两种抗心律失常药物如何影响心脏的不同部分。
副教授乔纳森•席尔瓦麦凯维工程学院生物医学工程,和珍妮Nerbonne,医学教授和发育生物学的医学院的领导的团队发现,两种药物,利多卡因和ranolazine,有时用来治疗心律失常,心中不同的工作根据表达的钠离子通道的分子组成。电压门控心肌钠(Nav),通道进行钠离子进入细胞,是至关重要的生成和传播通过心肌动作电位。自从大约10%的65岁以上成年人有心律失常,对潜在的治疗结果的工作有着广泛的含义。研究的结果发表在江森自控的洞察力2021年8月9日。
本机Nav渠道在心脏功能大分子蛋白质复合物,由单一导航α亚基,Nav1.5,生产Na +孔隙通道的选择性,和一个或多个细胞内和跨膜辅助蛋白质亚基认为影响渠道稳定、贩卖、本地化和/或属性。小组观察了两个导航的影响渠道附属子单元,β1和β3单元,利多卡因之间的交互和ranolazine Nav1.5-encoded频道。利多卡因和ranolazine,称为类1 b那儿有治疗潜力,但在一些患者无效的and-counterintuitively-raise心律失常的风险。
“心脏的病理可以跟亚基组成的变化来导航频道,”席尔瓦说。“如果一个人有一个不同的疾病和遗传背景,他们会有不同的钠离子通道组成比另一个人。”
席尔瓦的实验室在分子和细胞水平,工作和Nerbonne的实验室与小鼠模型和人类心脏组织,允许团队连接不同的生物。Wandi朱,论文的第一作者获得了生物医学工程博士学位2018年WashU,现在是哈佛大学研究员,在青蛙卵母细胞开始实验,她收集了非常详细的分子生物物理数据的属性Nav1.5-encoded渠道表达有或没有辅助β1和β3单元。Nerbonne实验室的成员一起,朱镕基对利多卡因的影响和ranolazine在老鼠心脏细胞钠通道有或没有β1亚基。Nerbonne的实验室分析β亚基的表达在老鼠和人类心脏组织。
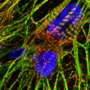
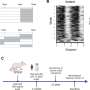
通过他们的实验中,他们发现这两种药物影响细胞膜电压传感组件Nav1.5的第三域,电子门打开和关闭钠离子通道,Nav1.5。β1亚基时,利多卡因比ranolazine更有效。然而,当β1亚基会缺席,ranolazine比利多卡因更有效。有趣的是,3β亚基了相反效果的存在,ranolazine更有效,而当缺席,利多卡因更有效。
此外,研究小组发现,β1亚基表达水平高出三倍的比人类心脏的心室心房,这表明分子组成的通道在这些不同的地区是不同的。
“这些差异,结合遗传或获得心血管疾病,极大地影响个体的反应病人Class-1b抗心律失常的治疗,”席尔瓦说。
Nerbonne说许多悬而未决的问题依然存在,所以他们的团队计划继续研究心脏Nav1.5-encoded渠道监管和在什么条件下了解辅助蛋白影响属性和心脏钠离子通道的功能。
“虽然抗心律失常drug-binding网站这两种药物都是一样的,当我们看到差异通道附属蛋白存在,”她说。“我们还不知道为什么,但它可能是这些药物Nav1.5绑定到其他网站,或者辅助β亚基的存在改变了结合位点,改变这些药物的影响。我们知道1 b类抗心律失常药物Nav1.5-endoded钠离子通道,所以区别可能是分子组成的通道。这些结果使一个非常合理的思考。”
以前,席尔瓦和他的团队研究了药物的功效美西律3型长QT综合征,在此期间他们发现领域三世voltage-sensing组件相关药物的效果。他们的模型显示,电压传感领域的转变至关重要的药物是有效的。
更多信息:朱Wandi et al,调制的影响Class-Ib那儿心脏NaV1.5-encoded频道副NaVβ子单元,江森自控的洞察力(2021)。DOI: 10.1172 / jci.insight.143092