通过蛋白质结构揭示了艾滋病病毒耐药性机制

索尔克研究所的研究人员,与美国国立卫生研究院的合作,已经发现的分子机制人类免疫缺陷病毒(HIV)成为抵抗Dolutegravir,最有效的,临床使用抗病毒药物治疗艾滋病。
7月21日发表的一项新的研究,2023年科学的进步揭示了如何整合酶的三维结构改变,艾滋病毒蛋白质,会导致Dolutegravir阻力和其他化合物可能会如何克服这种阻力。
“与艾滋病毒,必须认为前两个步骤病毒说:“索尔克副教授德米特里•Lyumkis文章的第二作者和赫斯特基金会发展的椅子上。“我们现在确定病毒如何继续发展对药物Dolutegravir一样,这也是需要考虑的重要的发展未来的疗法”。
艾滋病毒感染取决于病毒的能力将自己的遗传物质粘贴到的基因组人类细胞,本质上劫持细胞变成病毒制造工厂。Dolutegravir相关药物通过阻断整合酶,蛋白质的能力的关键病毒将自己的DNA整合到宿主基因组。没有功能整合酶,HIV病毒不能感染人类细胞。然而,艾滋病毒是一个快速变异的病毒,和越来越多的艾滋病病毒毒株是Dolutegravir耐药。
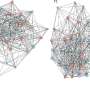
在过去,Lyumkis的实验室发现了整合酶的三维结构的蛋白质而DNA以及如何整合酶药物Dolutegravir绑定和块。但研究人员不确定如何整合酶结构改变当病毒Dolutegravir停止响应。
在新的研究中,Lyumkis和合作者的国立卫生研究院创建版本的整合酶蛋白与已知突变使Dolutegravir HIV耐药。
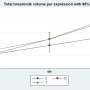
然后他们决定每个变异整合酶的结构,揭示为什么Dolutegravir再也无法绑定和块每个版本的蛋白质。科学家们还评估病毒的“适应性”(其传染性的后代生产能力)和酶的活动,以更好地了解导致耐药性在病人。
“我们非常惊讶的阻力的大小,这些整合酶变异,“Lyumkis说。“Dolutegravir功能的能力是完全妥协。”
研究人员还测试了一个实验性的功效艾滋病毒药物,4 d,阻止Dolutegravir-resistant整合酶蛋白的功能。4 d是由Lyumkis的合作者在美国国立卫生研究院新一代integrase-targeting药物,目前在临床前动物试验。
在所有的变种,他们发现4 d仍然有说服力地封锁了艾滋病毒基因整合到人体细胞的能力。这表明这种化合物的4 d或变异可能有效地用于治疗病毒在患者对Dolutegravir有了抗性。
结构数据4 d结合Dolutegravir-resistant整合酶蛋白也暗示新药如何克服耐药性。
“4 d只是如何对抗耐药性的一个例子,但它为我们提供了一些基本原则,我们可以从设计其他疗法,”文章的第二作者罗伯特·克雷吉说国家糖尿病、消化和肾脏疾病研究所(NIDDK),美国国立卫生研究院的一部分。“4 d分子栈的一部分像一个平板上的部分整合酶protein-DNA组装可以复制在其他化合物。”
接下来,科学家将研究如何整合酶变异evolve-including那些没有看到病人在未来——但可能如何影响反应最好的临床使用药物以及艾滋病毒感染人类的能力。
更多信息:李敏et al, hiv - 1整合酶抗dolutegravir机制和有效的抑制耐药变异,科学的进步(2023)。DOI: 10.1126 / sciadv.adg5953。www.science.org/doi/10.1126/sciadv.adg5953