研究揭示了预防肥胖驱动的肝损伤的潜在治疗方法
当一个肥胖的人开始积累肝脏中脂肪时,这种特别危险的健康风险是极其超重的。
这种情况 -非酒精脂肪肝病(NAFLD) - 世界上最常见的慢性肝病,是主要的基本原因肝脏移植在儿童和成人。没有这种移植物,只有只有一小部分患者可用,那么NAFLD随着时间的推移可能是致命的。事实上,(不包括酒精相关的肝脏损坏)每年超过30,000人死于NAFLD。
多年来,治疗NAFLD的主要方式是通过使用各种体重控制方法:饮食计划,运动方案,有限益处的药物,畜牧手术等。但是,一旦人们发展进步Nafld,就会简单地失去重量是不够的。
现在,经过多年的研究涉及肥胖症和NAFLD的众多机制,辛辛那提儿童报告中的20个科学家团队向前迈出了重要的一步。他们的研究结果是在线发布于2021年5月17日, 在细胞新陈代谢。
介绍初期的细胞
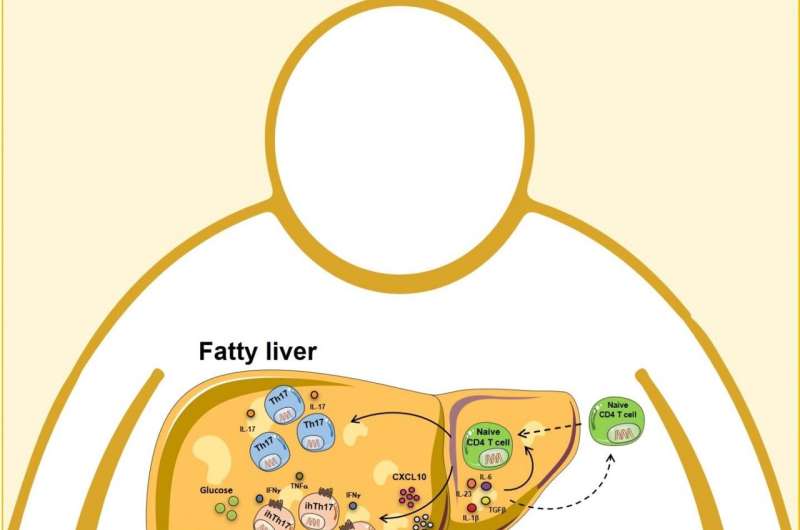
该研究小组报告说,由于肥胖导致的肝脏过度脂肪沉积可以改变肝脏的微环境,从而吸引高度特定的免疫T细胞群体细胞肝脏。这些“炎症性肝癌CXCR3 + TH17细胞”或“IHTH17”细胞继续引发过量的炎症和危及生命的肝脏损伤。
通过运行一系列实验使用人类组织和细胞和多条遗传修饰的小鼠,该团队发现肥胖本身沿着分子“途径”触发活性,该分子“途径”从CXC110和CXCR3基因的过量表达开始。这种异常活动吸引了较越来越多的IHTH17细胞到肝脏。结果是烧焦的地球炎症反馈回路,促进额外的免疫细胞并逐渐损害肝功能。
在追踪IHTH17细胞肝脏招募途径后,团队列出了找到一种破坏炎症不健康循环的方法。他们发现成功用小鼠造成的小鼠在其T细胞中缺乏基因PKM2的表达,这似乎对沿CXCR3途径的继续活性至关重要。
当这些改性的小鼠被诱导肥胖诱导饮食时,它们仍然有脂肪。但它们遭受的肝脏损失较少,而不是未修饰的小鼠。
接下来,研究人员测试了从NAFLD人们收集的人组织。他们证实,在人肝细胞中也可以检测到小鼠中发生的许多关键基因和分子活性。
“我们的结果首次证明了IHTH17细胞代表了NAFLD发病机制复杂世界的重要组成部分,”相应的作者说Senad Divanovic,Ph.D.是,辛辛那提和第一作者Maria Moreno-Fernandez,博士学位,Ph.D.,Divanovic实验室的博士生。
了解更多关于如何调节ihTh17细胞的功能,以及它们与肝细胞和免疫系统的相互作用,可能导致新的治疗方法,以减少NAFLD造成的伤害。
下一步
但是小鼠中使用的治疗方法也有助于人们吗?人类基因编辑不太可能随时是这种情况的可接受的选择。然而,Divanovic说,已知一些药物能够阻断PKM2活性。
这些药物仍需要更深入的实验室评估。最终,还需要在多年临床试验中进行有希望的化合物。但现在,在多年来,该团队有前途的探索。
“如果我们可以以目标方式调节与NAFLD相关的不需要的炎症反应,我们可能能够改善肝对NAFLD患者的生存和健康造成损害,”迪瓦诺维奇说。
进一步探索











用户评论