癌症药物载体的结构如何有助于选择性地靶向癌细胞
癌症的主要罪魁祸首是健康的细胞,已经流氓,并获得无法控制地分裂的能力。这些细胞通过正常细胞获得生长优势,并通过改变参与生长和代谢的细胞途径来操纵它们的环境。在过去的几十年中,各种改变的途径和蛋白质已被鉴定为治疗干预的靶标。然而,仍然有挑战性的是选择性靶向癌细胞,并确保药物以足量达到肿瘤,而不会严重影响正常细胞。在这方面,生物相容性递送载体(对正常细胞无毒)可以是有用的。
一种这样的潜在候选者是卟啉,一组有机环状化合物,其在人体中形成几种蛋白质的功能中心。卟啉以其光敏效应而闻名,即它们的释放能力反应性氧气轻刺激。这些反应性物种是给卟啉的抗癌活动。卟啉具有另一个优点:在结构上,它们由称为吡咯亚基的四个亚基组成,其为它们提供特定的电子特性。这些电子性质与受体组合癌症细胞,促进卟啉在癌细胞中的选择性积累,从而用作有效药品输送系统。但是如何与卟啉结合的官能团的空间位置(原子排列)最大限度地积累和分布卟啉- 癌细胞中的缀合物尚未得到很好的研究。
为了回答这个问题,东京科学大学的研究人员包括助理。Toshifumi Tojo教授,Koshi Nishida先生。Takeshi Kondo教授和Makoto Yuasa教授深入挖掘卟啉衍生物的结构如何影响肿瘤积累。他们的调查结果在期刊上发表科学报告。领导这项研究的Tojo博士解释了他们的动机,他说:“由于卟啉在癌细胞中积累的能力,所以卟啉被用作癌症治疗新药的基本框架。它们对药物偶联具有不同的官能团修饰位置。这些部位是否具有不同的物理性质和膜通透性尚不清楚。我们的目的是调查这些差异如何影响给药。”
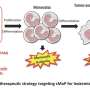
在他们的研究中,研究人员探讨了卟啉中官能团的β(第三)和Meso(中间)位置。首先,使用乳腺癌细胞系,他们研究了这些功能位置如何影响时间依赖的积累癌细胞,范围从2到24小时的时间点。他们发现,比β-衍生物高出3倍的细胞中累积的中间衍生物,并且具有较小官能团的衍生物允许比较大的衍生物更好。
接下来,他们研究了这些功能群体的位置如何影响卟啉进入癌症呼叫的途径。他们发现卟啉缀合物与血浆蛋白质的复合物,其通过内吞囊泡促进其运输。另外,化合物还可以通过细胞膜扩散到细胞质中。
此外,考虑到它们的电子性质,卟啉可能与将它们运送到细胞的血清蛋白质相互作用。因此,研究人员测量了不同的位置如何影响这些卟啉缀合物与血清蛋白质的亲和力以及如何提高肿瘤积聚的增加。他们发现,虽然中间位置改善卟啉缀合物的细胞内积聚,但它对小的运动没有重大影响功能群体进入细胞。
结论他们的研究结果,博士讲话,“我们的研究表明,卟啉的官能团修饰位置极大地影响了膜渗透性和细胞内肿瘤积累。我们希望我们的调查结果可以帮助为新型卟啉的结构设计提供信息毒品。“
总体而言,他们的研究能够深入了解卟啉如卟啉如卟啉的结构如何实现最大疗效,希望为癌症药物递送的进步铺平途径。
进一步探索














用户评论