研究有助于铺设新批准的药物
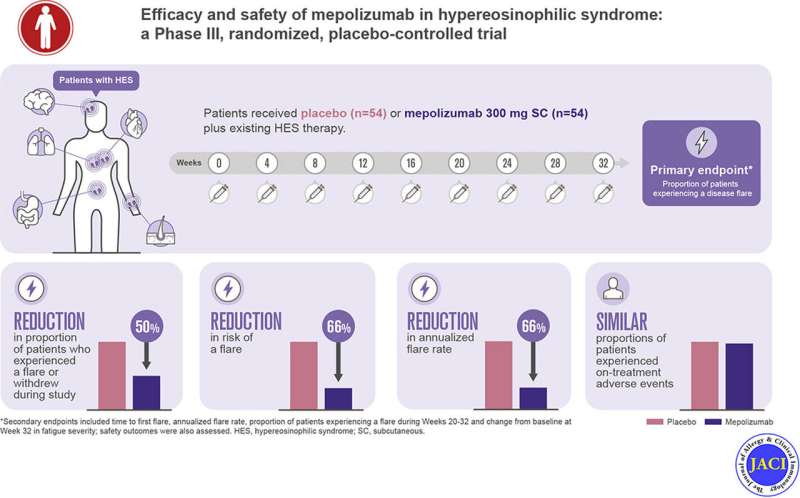
在美国食品和药物管理局在辛辛那提儿童医院医院医疗中心的一组罕见的疾病研究中,美国食品和药物管理局已批准用于治疗过嗜酸性综合征患者的药物Nucala(Mepolizumab)。
综合症综合征,也称为他,是一种危及生命的血液疾病组,涉及具有高水平嗜酸性粒细胞,一种在免疫系统中起重要作用的白细胞。随着时间的推移,这些过高水平的嗜酸性粒细胞进入组织和器官并导致损坏。到目前为止,高剂量的皮质类固醇用于降低嗜酸性粒细胞水平以防止损伤器官。然而,疾病耀斑仍然发生,这些疾病耀斑对身体造成危险损害。
这FDA在9月25日新闻发布中陈述原子能机构已批准Nucala(Mepolizumab)为12岁或以上的患者六个月或更长时间或更长时间,没有另一种可识别的非血液相关原因的疾病。
“我们在辛辛那提儿童获得了一个家庭奔跑,因为我们通过我们的研究代表患者追求这两十年,”Marc Rothenberg,Md,Ph.D.,Marc Rothenberg,Marc Rothenberg表示,博士学位和辛辛那提司司长兼辛辛那提儿童嗜酸性疾病中心。
“我们专注于嗜酸性疾病而且这对患者来说是一个很大的突破,“罗斯伯格涉及相关翻译研究和莫比利司布的临床试验,以前的FDA批准。”含有罕见疾病的人必须真正争取改善的治疗和他们的标签批准,这是一个漫长的旅程。“
Mepolizumab,阻断嗜酸嗜酸性粒细胞生长因子IL-5的生物抗体,于2015年被批准为哮喘药物。
FDA批准治疗过苯磺酸综合征的手段“患有HES的患者有一种治疗选择,将减少疾病的味道,并且具有改善的健康,而没有本药的实质性副作用,”Rothenberg说。
Rothenberg侧重于他的实验室对阐明过敏反应机制的研究,尤其是粘膜组织如胃肠道和肺。
对Rothenberg的研究已经包括来自嗜酸性疾病(治愈)的竞选研究的竞选研究,这欢迎FDA批准的新使用Mepolizumab的新闻。
“这项决定对患者及其家人来说意义重大,”Ellyn Kodroff,创始人和嗜酸性疾病敦促研究竞选研究总监Ellyn Kodroff说。“拥有FDA批准使患者能够提供保险范围的药物,给予更好和更长的生活。痊愈是因为培养和捐赠了数百万美元的资金转化研究,以靶向嗜酸性嗜嗜酸性条件的理由,如Mepolizuab是否。这种持续的研究支持罕见的嗜酸性疾病的未满足需要是生命变化。“
Rothenberg于20世纪90年代开始研究哈佛大学的博士生。当时他表明IL-5参与人类疾病及其对嗜酸性粒细胞的影响。
在辛辛那提儿童的,Rothenberg以及世界各地的其他研究人员以及嗜酸性粒细胞均为过敏性疾病的促炎细胞提供了证据。Rothenberg和他的同事促进了靶向嗜酸性粒细胞的理由,包括表演临床研究在患有各种嗜酸性疾病的患者中。
2008年,Rothenberg领导了国际调查人员进行了随机临床试验,证明了Mepolizuab对HES患者患者的低口服类固醇剂量的能力(Rothenberg等。新英格兰医学杂志2008年3月20日; 358(12):1215-28。DOI:10.1056 / NEJMOA070812。EPUB 2008 3月16日PMID:18344568)。
罗斯伯格说,尽管符合该研究的主要终点,但FDA收紧了Mepolizumab的批准标准。最终会达到FDA所要求的终点,专注于在这种稀有疾病人群中的临床益处,额外研究了额外的研究。
如最近的出版物中所述过敏与临床免疫学杂志在第3阶段,随机化,安慰剂对照试验中的青少年和成年患者调查Mepolizumab的疗效和安全性,显示Mepolizumab,减少了HES疾病耀斑的数量(roufesse.等。过敏与临床免疫学杂志2020年9月18日;S0091-6749(20)31276-8。DOI:10.1016 / J.Jaci.2020.08.037。)。该试验中的108名患者来自39个中心和13个国家。











用户评论