科学家建立新型“Kuma突变”小鼠永久性新生儿糖尿病模型
糖尿病很少发生在新生儿 - 一种称为新生儿糖尿病的病症。但是,当它确实时,它主要是由于单个基因中的突变,例如KCNJ11或胰岛素(INS)。这种早期出现的糖尿病类型与1型糖尿病不同,因为它发生在寿命的前六个月内,并且可以是瞬态或永久性的。根据这种疾病的大多数突变可防止胰腺产生足够的胰岛素,这导致高血糖水平或高血糖。
了解什么导致永久新生儿糖尿病为了找到治疗方法,科学家们经常使用胰岛素2 (Ins2)C96Y基因突变的老鼠和猪模型。这些模型发展为类似新生儿糖尿病的永久性早发糖尿病。然而,这些模型的一个主要局限性是,通过使用它们,物种间的胰腺胰岛素生产移植细胞(胰腺β细胞)不能评估称为胰岛移植,由于表征这种梭菌移植的不利免疫系统反应,不能评估。
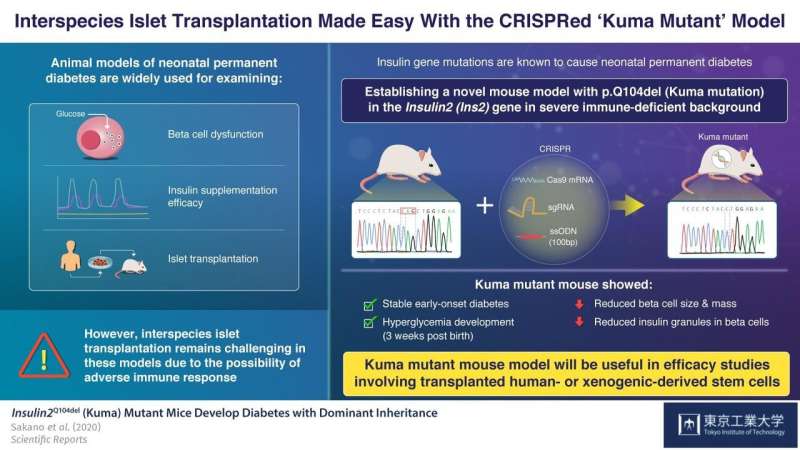
现在,在发表的文件中科学报告,来自东京技术的科学家描述了他们如何建立新的小鼠模型在免疫缺陷背景下表现出严重的胰岛素缺乏和β细胞功能障碍的永久性新生儿糖尿病。正如领导这项研究的Shoen Kume教授解释的那样,“我们想创建一个小鼠模型,使我们能够评估移植人类干细胞或异种干细胞的功效。胰腺β细胞而不用考虑免疫反应。”
为实现这一目标,科学家们使用CRISPR / CAS9基因编辑技术在严重免疫缺陷BRJ小鼠的INS2基因中引入三个碱基对缺失,缺乏成熟的T和B淋巴细胞和天然杀伤(NK)细胞。该突变导致GLN(Q)缺失(P.Q104DEL),阻碍胰岛素产生。科学家们命名为突变“康马突变”。
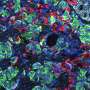
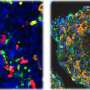
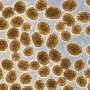
在对熊氏小白鼠进行衰老检查后,科学家们发现,雄性和雌性突变熊氏小白鼠在出生三周后都出现了高血糖。他们推测这可能是由于突变的胰岛素蛋白稳定性较低所致。科学家们还注意到,这些小鼠的β细胞面积、大小和质量显著减少,β细胞内胰岛素颗粒的数量和大小也显著减少。这意味着老鼠可以作为永久的新生儿糖尿病胰岛移植模型。
为了证实这一点,他们的治疗方法胰岛素植入物超过四周成功逆转其高血糖。
基于这些发现,Kume教授和他的团队认为,“Kuma突变体不仅可以用于胰岛素基因和β细胞功能障碍的分子研究,而且其免疫缺陷背景使其具有吸引力。模型用于检测由人类或异种干细胞产生的移植β细胞的功能。”
此外,由于Kuma突变在不同物种之间保存良好,同样的基因编辑方法可以应用于在其他动物物种中创建永久性新生儿糖尿病模型,使这种疾病的研究进展更容易一些。
进一步探索











用户评论