临时盐晶可以为阿尔茨海默氏症提供永久性溶液
阿尔茨海默病是痴呆症全球的主要原因和残疾的主要原因。现在,大阪大学和北海道大学的研究人员表明,即使在纳米级的低盐浓度下,也会发生盐晶的重复沉淀溶出事件,并且它可以加速神经毒性淀粉样蛋白-β肽的聚集在其发病机制中。
这人脑包含约860亿神经元,大致像大型自卸卡车一样多的沙粒。这些神经元将电化学信息作为大脑,肌肉和器官之间的信号,以协调生存与自我意识的生存。阿尔茨海默病的疾病破坏了这种复杂的神经元网络,导致功能性残疾和细胞死亡。尚未保证,可用的护理是对症,支持或姑息的;理解其发病机制的突破可能会照亮药物,诊断和预防的前景。
淀粉样蛋白在阿尔茨海默病中的作用长期以来一直被认可。淀粉样蛋白-β肽衍生自淀粉样蛋白前体蛋白它们自组装成尺寸,从低分子量聚集体和较大的低聚物到淀粉样蛋白原纤维。众所周知,这是神经毒性的,但最近的研究表明,寡聚病症的聚集体也是毒性,可能甚至超过原纤维。
“原纤维聚合从成核开始,然后是一个伸长阶段,“克里基塔罗纳哈吉玛解释,本研究的铅作者。”直到现在,由于它们的形态变异性,核心的时间框架,难以研究的寡头聚酰胺进化的早期阶段,以及核心的时间框架,以及缺乏合适的荧光测定。“
-

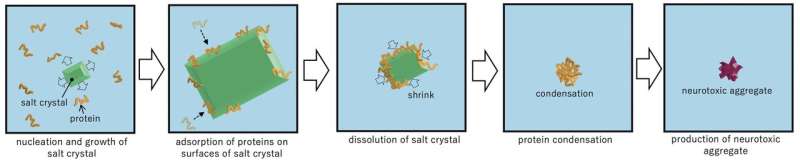
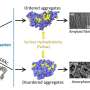
图。图2示出了由液态传输 - 电子显微镜观察到的盐晶的沉淀溶解事件的图像。信誉:大阪大学 -
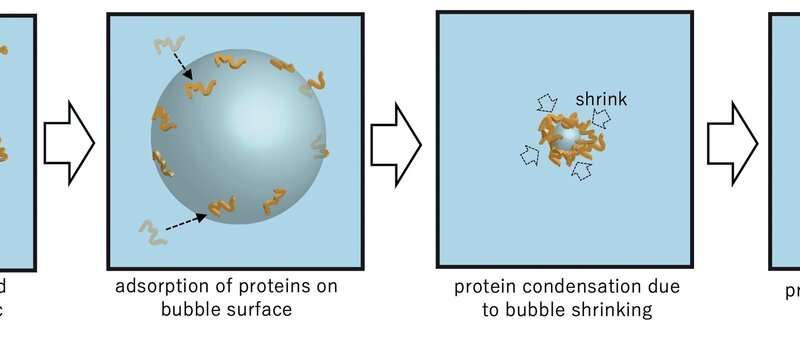
图3超声波空化蛋白质聚集加速机制。信誉:大阪大学
使用液态透射电子显微镜检查,研究人员分析了蛋白质分子的聚集,获取了时间分辨的纳米级图像和电子衍射图案。“显着的是,我们发现即使在局部密度波动的浓度低于其浓度下,盐晶也可以沉淀,并且其快速溶解加速了淀粉样蛋白-β肽的聚集反应,”相应作者Hirotsugu Ogi教授说。“这种临时盐晶的形成提供了一种机制,蛋白质粘附到晶体的表面;当它溶解时,界面收缩,在消失点处冷凝蛋白质。这种现象类似于超声波空化泡的聚集加速度。附着蛋白质在膨胀相期间在气泡表面上,它们通过其中心的超声波的正压塌陷,它们高度冷凝。这是人工催化作用。因此,在自催化的纳米镜的聚集机制中,盐溶解加速聚集反应,骨料本身可以促进盐成核。“
OGI解释了它们的结果的影响:“淀粉样蛋白-β肽的聚集缓慢,这是药学研究的障碍。建立有效的加速度方法将有助于阐明他们对原纤维的单体的结构演变。理解是关键阿尔茨海默病的发病机制。“















用户评论