末梢病变——寄生细菌如何诱导血管形成引起病变
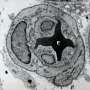
巴尔通体属细菌是一种寄生虫,可通过昆虫叮咬和动物抓伤传播给人类,导致巴尔通体病。猫抓病和壕热是巴尔通体病的两种形式,由感染人类的不同巴尔通体物种引起。巴尔通体细菌会导致皮肤和内脏器官出现病变。为了给自己提供一个安全的栖息地,细菌带来了血管内皮细胞(排列在血管内部的细胞)数量的增加,这些细胞将自己隐藏起来,不被宿主的免疫系统发现,并通过一个称为血管生成的过程刺激新血管的生成。
先前对导致猫抓病的巴尔通体(Bartonella henselae,简称B. henselae)的研究表明,它可以直接“注射”抑制编程的蛋白质细胞死亡(细胞凋亡)进入内皮细胞细胞.然而,B. henselae也可以在不直接接触内皮细胞的情况下促进血管生成,这意味着该细菌可以分泌一种生物活性物质,承担启动血管生成的职责。
一项新的研究发表在自然通讯,由日本藤田卫生大学的高级助理教授冢本健太郎和Yohei Doi教授领导的科学家团队已经确定这种生物活性物质实际上是一种蛋白质.他们还将这种蛋白质命名为巴尔通体血管生成因子A,简称BafA。这是第一次报道血管内皮生长因子(VEGF)样蛋白由细菌.
科学家们通过将B. henselae引入人体内皮细胞开始了他们的项目培养皿,并观察到细菌引起内皮细胞的繁殖。为了确定赋予B. henselae这种能力的基因,研究人员开始在细菌的DNA中诱导随机突变,并观察突变的细菌是否仍然可以使内皮细胞繁殖。通过这些实验,科学家们确定,只有当B. henselae拥有编码或指导BafA蛋白合成的基因的功能副本时,它才能刺激人类内皮细胞的血管生成。他们还观察到,将人内皮细胞暴露于分离的BafA蛋白会导致细胞繁殖。
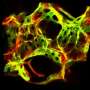
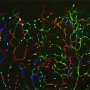
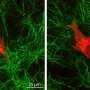
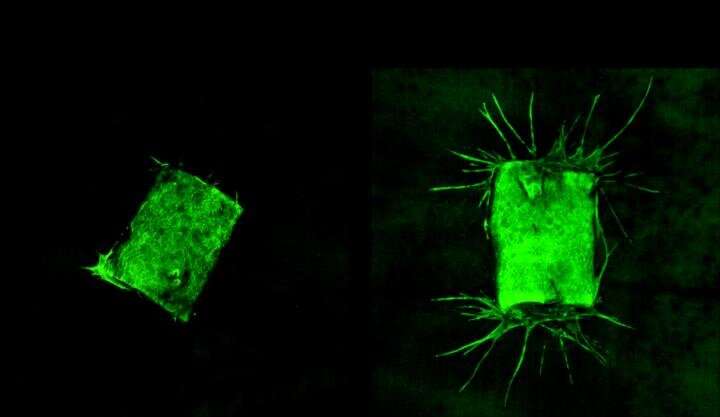
然后,为了证实BafA刺激血管生成,科学家们从老鼠身上提取了一种叫做主动脉的主要血管样本,并将样本放在含有或不含BafA的凝胶中。从下图中可以看出,未暴露于BafA的主动脉样本没有长出新的血管,但暴露于BafA的主动脉样本长出了延伸到凝胶中的血管。科学家们还发现,通过外科手术将含有bafa的凝胶塞植入活体小鼠体内,可以使血管从周围组织生长到凝胶中。
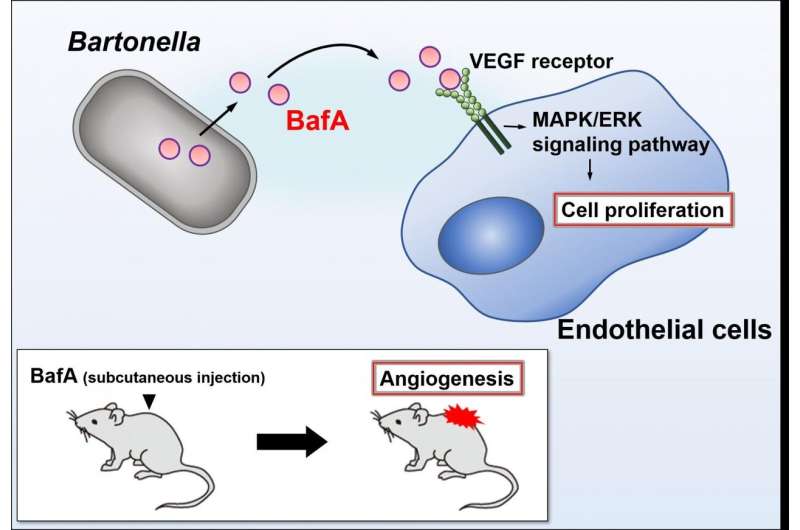
在培养皿中对人内皮细胞的进一步实验表明,BafA激活了识别VEGF的细胞表面受体。通过与这些受体结合,BafA触发了细胞内一个过程的激活,涉及称为丝裂原活化蛋白激酶(MAPK)和细胞外信号调节激酶(ERKs)的蛋白质。MAPK/ERK通路在内皮细胞增殖和血管生成中起着重要作用。“在最后一组实验中,我们对一种名为昆塔纳巴尔通体的相关细菌进行了类似的研究,这种细菌会导致堑壕热,我们发现它会产生自己的BafA版本,也会导致人类内皮细胞冢本博士解释道。
这些发现为感染性细菌在宿主体内产生病变的机制提供了有价值的见解。Doi教授报告说:“我们相信BafA蛋白可以作为研究血管生成的工具,我们也考虑到潜在的医疗效益。”“最重要的是,”他解释说,“BafA是开发巴尔通体病诊断和治疗策略的潜在目标。”
科学家们还推测,BafA蛋白可以用于再生医学,这是一个高度专业化的医学分支,用于替换或再生身体失去或受损的部分。需要进一步的研究来证实科学家的发现,但毋庸置疑,BafA蛋白肯定会引起科学界的极大兴趣。
更多信息:Kentaro Tsukamoto等人,巴尔通体自转运体BafA激活宿主VEGF通路以驱动血管生成,自然通讯(2020)。DOI: 10.1038 / s41467 - 020 - 17391 - 2