研究人员开发了新的微针阵列组合疫苗传递系统

匹兹堡大学医学院(University of Pittsburgh School of Medicine)的研究人员目前正在研究一种潜在的冠状病毒疫苗,与此同时,他们开发了一种新的疫苗输送系统,用于使用活病毒或减毒病毒载体接种疫苗:一个手指大小的贴片,包含400个微型针头,每个针头只有0.5毫米。报道了他们的进展调查皮肤病学杂志。
由糖制成的针和递送的特定货物,包括三维(3-D),多组分溶解微针阵列(MNA)。虽然感觉像魔术贴皮肤,疫苗会渗透皮肤的上层,吸收皮肤的水分,然后溶解和释放促使的分子免疫系统使抗体攻击病毒。除了抗体生产外,该技术还有可能改善患者的细胞免疫应答,并扩大全球免疫能力。这是清楚的证据表明皮肤科学家的广泛覆盖和贡献,甚至延伸到大流行疫苗设计。
解释这项工作的重要性,领先作者路易斯D. Falo,Jr.,MD,博士,匹兹堡大学医学院和UPMC学院皮肤科教授和主席,美国匹兹堡,帕茨堡,美国解释说,“我们正在开发这种新的递送技术,因为传统疫苗往往有效地诱导抗体反应,它们经常无法产生预防或治疗许多癌症或治疗许多癌症必不可少的细胞反应传染病。"
皮肤是一个理想的接种地点,因为它包含一个高度敏感的免疫网络,并鼓励产生强大和持久的免疫力。
可溶解的MNAs被设计成机械地穿透表层皮肤,插入皮肤后迅速溶解,并将均匀数量的生物物质输送到皮肤内定义的3-D空间。这使得在这个特定的皮肤微环境中,能够局部传递少量的药物或疫苗以达到高浓度。
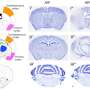
利用体内小鼠模型,研究人员生成了3-D多组分可溶疫苗平台,将活腺病毒编码抗原与添加的组分聚肌苷:聚胞苷酸(poly I:C)结合起来,这是一种用于模拟皮肤免疫系统的免疫刺激剂。这成功地诱导了抗体反应和更强的细胞免疫反应。
抗原特异性细胞免疫的诱导是疫苗领域的强调点,通过靶向感染细胞产生“普遍存在的传染病等可变感染疾病的”通用疫苗“的努力证明。
“非常”,“Falo博士说,”掺入抗原编码的腺病毒和多I:C的MNA疫苗平台,与单独的腺病毒的MNA递送显着减少了靶细胞的破坏。“研究人员还发现,MNA整合到Poly I:C和腺病毒在4个月储存后保留了其免疫原性?C.与其他疫苗输送平台相比,MNA递送的疫苗还具有易于制造,应用和储存的优点。
Falo博士评论说:“我们的结果表明,多组分MNA疫苗平台能够将佐剂和抗原编码病毒载体同时传递到相同的皮肤微环境,从而提高免疫原性,包括细胞免疫应答。”“这种MNA递送方法可以提高目前正在开发的用于预防冠状病毒病(COVID-19)的腺病毒疫苗的有效性。”














用户评论