同系免疫活性宿主中前列腺癌骨转移的小鼠模型
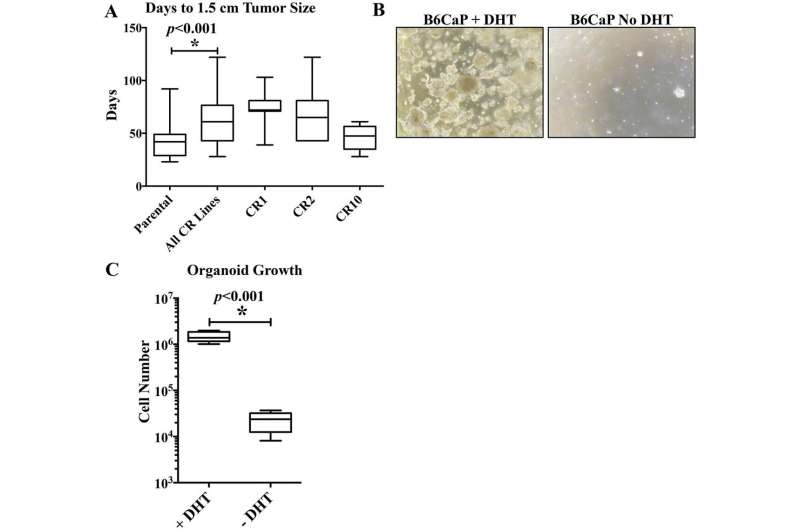
研究小组报道了B6Ca P的建立,这是一种来自Hi-Myc转基因小鼠的同种异体移植肿瘤系,该肿瘤系已经回交到C57BL/6J背景上。
这是第一个前列腺源性肿瘤的例子,显示频繁的骨转移和生长在免疫功能良好的宿主,使之模型有助于研究骨转移和肿瘤免疫反应的机制。
博士博士,来自泌尿外科,西北大学福内伯格医学院的泌尿外科,芝加哥,伊利诺伊州,“前列腺癌(PCA)是美国最常见的非皮肤癌,是第三个男性癌症相关死亡原因。“
癌症的动物模型允许研究疾病进展的分子机制,并在疾病部位测试新治疗;但罕见的自发发生前列腺癌在小鼠和缺乏动物模型系统来紧密概括人类前列腺癌阻碍了转移进展的机制理解和发展有效的晚期前列腺癌治疗。尽管在免疫缺陷小鼠中移植人类细胞系仍然是最常用的模型,但除了少数细胞系在原位注射时发生转移外,PCa细胞系很少从皮下移植物转移。
为了克服这些问题,多年来,许多转基因PCA的基因工程鼠标模型包括将PCA转移的流浪模型显示到肺等遥控器,但很少是骨骼的特征转基因小鼠模型。
Intracard in注入B6CA P导致频繁的骨骼转移,使其成为研究PCA转移机制的优异的临床前模型。
Schaeffer研究小组总结说,总的来说,B6Ca - P系克服了研究前列腺骨转移的两个关键限制癌症。
进一步探索














用户评论