按需制作血液:我们来了多远?
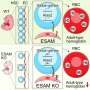
人类血液系统的重建具有良好的治疗潜力,可以治疗许多疾病,如血液癌,镰刀细胞贫血等。成功的重建需要造血(或血液)干细胞(HSC)的移植和植入,在到达其Niche后,开始产生所有类型的血细胞,包括血小板,白色和红细胞。
在目前的临床实践中,这是由注入肝星状细胞获得一个匹配的捐献者免疫兼容病人需要(同种异体移植),或通过病人自身的肝星状细胞的扩张在实验室里,然后re-infusing他们回病人(体外,自体移植)。然而,这两条线路的效用目前受到一些因素的限制。首先,在同种异体移植的情况下,匹配供体的稀缺显著增加了等待时间,这可能对患者不利。其次,由于造血干细胞有限的增殖潜能,无论是异体造血干细胞还是自体造血干细胞的体外扩增一直是一项具有挑战性的任务细胞展览文化。这些限制已经提出了对其他HSC来源的需要,这将减轻对匹配的供体的需求并大量产生官能HSC。
在2007年,三田山塔教授和同事们展示了这一点体细胞如皮肤成纤维细胞,可以重新编程回类似的蜂窝状态人胚胎干细胞(HESC),这是一群在胚泡阶段人胚胎中发现的细胞,并仅促进妊娠期间的人类胎儿的发展。将重编程的细胞称为诱导多能干细胞(IPSC)。除了其发育潜力外,人体ESC和IPS细胞还显示出培养的无限增殖性潜力,这使得它们通常是再生医学的理想细胞来源,并且用于造血分化以获得可能无限量的HSC。因此,利用这些细胞治疗血液疾病的潜力,已经存在越来越感兴趣。
然而,来自人多能干细胞的衍生功能HSC的进步已经缓慢。这归因于对正常血液缺陷的分子机制不完全了解。在本次审查中,作者讨论了产生能够长期植入和重建的HSC的最新努力血液来自人多能干细胞的系统。在过去几年中,干细胞研究在该地区见证了这一领域的里程碑成就,其意义是详细讨论和分析的重要性。
作者另外讨论了血液血症和造血分化,Homeobox(Hox)和Gata蛋白的背景下讨论了两个非常重要的转录因子。这些被认为是母体监管机构,在具有许多转录目标的意义上,在激活后,可以引起细胞身份的显着变化。作者假设造血分化期间这些家庭某些成员水平的精确时间控制可以产生能够长期植入的功能性HSC。
作者将审查结束了未来观点的摘要,其中他们讨论了新开发的技术如何在多能程化的造血分化过程中使用如去激活-CAS9(DCAS9)基因表达控制系统。干细胞为了精确的时间控制上述主调节器以实现功能性HSC。
进一步探索












用户评论