科学家发现了心脏正确收缩和存活的必要蛋白质
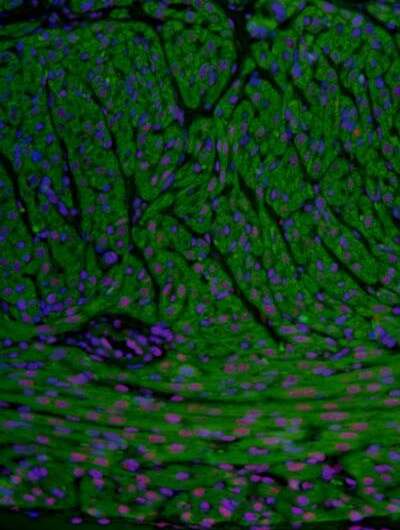
心血管疾病是世界上主要的死亡原因。仅2015年,就有1770万人死于心血管疾病,其中670万人死于心脏病发作。不幸的是,关于分子机制调节a心肌梗死,阻碍了新的治疗方法的发展。最近大规模信使RNA (mRNA)测序技术的发展已经允许识别与心脏病发展相关的基因表达模式。然而,对转录后调控(一种基因调控)的了解仍然有限,特别是rna结合蛋白(RBP)在心肌梗死和心脏病发展中的作用。
rna结合蛋白在细胞中执行重要的任务。“在这项研究中,我们调查了RBP SRSF3在心脏中的作用,这是迄今为止未知的,”Lara Pezzi博士解释说。
研究第一作者Dr. Paula Ortiz Sánchez与研究团队的其他成员一起发现,在胚胎发育期间,SRFS3在心肌细胞中高水平表达,并调节其分裂。“这些细胞中缺乏SRSF3的胚胎会死亡,”Lara Pezzi博士说。但在成人心脏中,“心肌细胞几乎不分裂,SRSF3的表达要低得多,特别是经过a心脏病这表明SRSF3在成人心脏中的作用肯定是不同的。”
作者开发了一种转基因小鼠模型这使得他们能够在特定的时间特异性地消除SRSF3在心肌细胞中的表达。科学家们发现,成年肌细胞中SRSF3的清除有一个显著的效果,严重损害了心脏收缩。
为了研究SRSF3支持心脏收缩的机制,该团队比较了缺乏SRSF3小鼠心脏中表达的所有mrna的表达模式和选择性加工(剪接)与对照小鼠的结果。“我们发现了表达式编码肌节(心肌细胞内的物理收缩装置)蛋白质成分的mrna水平,”Pezzi博士解释说。“SRSF3缺失的减少是由于这些mrna的降解,这是由于mrna 5'端被称为“帽”的化学修饰缺失造成的,除了其他功能外,该修饰还可以保护mrna不被降解。”
进一步的实验表明SRSF3控制着mTOR的选择性加工,mTOR是细胞代谢的主要调节因子。“在没有SRSF3的情况下,一个更短版本的mTOR被表达。这种缩写形式是无功能的,并导致mtor调节蛋白的一系列化学变化。结果是编码肌节蛋白的mrna的帽丢失,导致它们的降解和在srsf3缺陷小鼠中看到的严重收缩缺陷。”
识别mRNA封盖作为一种机制,以防止收缩的发展心如果失败,可能会为开发急需的治疗工具来对抗这种疾病开辟道路。
进一步探索















用户评论