研究发现巨噬细胞的途径培养PTEN缺乏胶质母细胞瘤
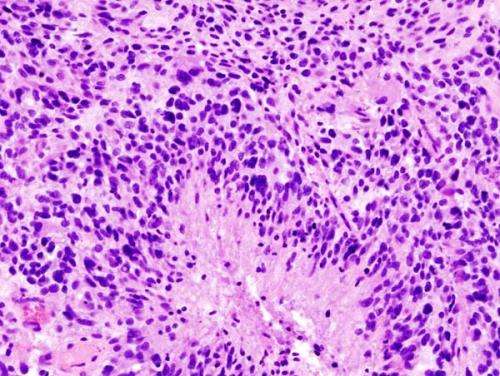
常见的遗传缺乏赋予胶质母细胞瘤以向错误类型的免疫细胞播放分子信息,召唤巨噬细胞,保护和培育脑肿瘤而不是攻击它,德克萨斯州和德斯逊大学癌症中心报告中的研究人员癌症细胞。
该小组在小鼠模型上的工作胶质母细胞瘤缺少功能性的癌抑制基因PTEN,为治疗最常见和致命的大脑指明了新的潜在靶点瘤据称,M.D.,M.D.,M.D。,M.D。,M.D。,M4D。,M.D.,MD.。
大约三分之一的胶质母细胞瘤缺乏pten。胶质母细胞瘤的中位生存期约为12至15个月,只有5%的患者能存活5年。
“我们已经确定了一个在pten缺陷的胶质母细胞瘤中被激活的共生回路,它在进入胶质母细胞瘤的癌细胞和巨噬细胞之间创造了相互支持的关系肿瘤微环境并为肿瘤提供生长因子支持,”徳平厚说。
巨噬细胞吞噬和消化微生物,细胞碎片和肿瘤细胞作为免疫反应的一部分,它们分泌影响其他的细胞因子细胞。他们是双相。以M1的形式,它们积极协助免疫反应并抑制肿瘤生长。在M2中,它们处于修复模式,帮助免疫后恢复,这也可以促进癌症的生长和发展。
胶质母细胞瘤中多达一半的活细胞是巨噬细胞。研究人员指出,它们是形成肿瘤微环境的主要成分。
第一作者陈培文博士,癌症生物学博士后,徳平厚博士和他的同事们开始寻找与肿瘤微环境免疫变化相关的胶质母细胞瘤的共同突变。
他们不仅确定了巨噬细胞进入胶质母细胞瘤的途径,而且还确定了由巨噬细胞分泌的一种生长因子,从而起到保护作用癌症细胞从编程的细胞死亡和燃料中的新血管的生长。
“我们首先发现只有PTEN缺乏,而不是其他共同的遗传改变,与胶质母细胞瘤中的巨噬细胞浸润有关,”陈说。
在一系列实验中,在Pten敲除细胞系中,后来在胶质母细胞瘤的小鼠模型中,它们显示出:
- 随着PTEN,一种称为YAP1的基因被激活,转录因子增加LOX的表达,这是一种新的巨噬细胞吸引物;
- LOX连接到巨噬细胞上的β1整合素- pyk2通路,刺激它们迁移到肿瘤微环境;
- 巨噬细胞通过分泌生长因子SPP1直接帮助胶质瘤细胞,研究小组发现这种生长因子可以增加癌细胞存活和血管形成,从而保护肿瘤。
挫败LOX缩小肿瘤,阻止巨噬细胞渗透
该团队开发了具有高表达LOX、YAP1和巨噬细胞标记物的人脑胶质母细胞瘤异种移植小鼠模型。在这些模型中,使用shRNA、小分子LOX抑制剂BAPN或抗LOX抗体消耗LOX受损肿瘤的生长并显着降低巨噬细胞渗透。
LOX抑制四种pten缺陷的胶质母细胞瘤小鼠模型延长了所有模型的生存。
阻断LOX对胶质瘤细胞增殖没有影响,但确实增加癌症细胞编程细胞死亡并降低肿瘤支撑血管的形成。
作为对他们的发现对人类可能产生的影响的第一次检查,该团队对癌症基因组图谱中的489个人类胶质母细胞瘤样本进行了无监督的巨噬细胞聚集。
通过巨噬细胞高(201),巨噬细胞培养基(153)和巨噬细胞低(135)组的聚类病例,以及与来自胶质母细胞瘤小鼠模型和患者的血液衍生的单核细胞相比分析肿瘤相关的巨噬细胞,它们确定了八个基因与患者巨噬细胞浸润相关。在八个中,SPP1是表达式最大的基因。
巨噬细胞高组具有更频繁的PTEN突变或缺失,较高的YAP1和LOX表达以及巨大的存活率而不是巨噬细胞低簇中的患者。
LOX,SPP1是PTEN缺乏胶质母细胞瘤的新目标
Depinho表示,途径中最具靶向的组成部分是LOX和SPP1,并在发育中的药物来击中两个基因。
徳平厚说:“在老鼠身上的结果已经足够令人信服了,而在人类胶质母细胞瘤上的相关研究为在复发性胶质母细胞瘤患者的临床试验提供了额外的信心。”
他说,只招募那些PTEN缺陷肿瘤的患者是很重要的,因为他们的研究表明,LOX抑制对野生型PTEN肿瘤不起作用。
进一步探索













用户评论