器官的形成如何帮助干细胞研究人员开发糖尿病和癌症的未来治疗方法
在一项新的研究中,哥本哈根大学的研究人员表明,一种特定类型的未成熟干细胞(也称为祖细胞)的发育取决于一种特殊蛋白质的数量以及与体内其他细胞的相互作用。这项新研究刚刚发表在科学杂志上细胞发育。
许多疾病是由于丧失某些类型的细胞例如,糖尿病患者体内产生胰岛素的细胞,或者是细胞功能障碍,例如癌症。干细胞研究人员多年来努力恢复正常健康的细胞类型。然而,问题是如何诱导干细胞在体内培养皿中的表现相同的方式。
更靠近可以控制蜂窝发育的机制
哥本哈根大学的SEMB集团旨在了解胰岛素的发展方式β细胞在胰腺中自然形成,从而可以在实验室中复制该过程。
“我们检查了多少祖细胞随着胰腺发生的胰腺发生,如果他们在器官内的不同区域(所谓的利基)的旅程可以解释他们最终将成为的东西。我们发现在祖细胞已经决定他们之前命运,他们走到了很多东西。我们还可以表明他们对特定利基的运动,他们获得最终命运的特定利基,由它们产生的蛋白质p120ctn中的大量策略决定。通过了解这种机制,我们可以提高我们从中制作正确的细胞类型的方法干细胞在培养皿中用于未来的细胞替代疾病,如1型糖尿病,并进入如何防止癌症传播的新洞察,“Henrik Semb,Nortonisk Semboroloology of Nortisk Semb,Lego Nordisk Foundation中心,哥本哈根大学Danstem。
细胞命运决定了细胞的粘痕
恢复功能失调的器官需要了解器官形状如何形成及其对细胞命运的影响。先前的研究得出了相互矛盾的结果。一些结果表明,祖细胞的未来命运是预先决定的,也就是说,祖细胞的命运在其最终的生态位之前由遗传决定,而另一些结果则相反,即祖细胞的命运在其最终的环境目的地被决定。
“因此,我们决定通过更详细地检查祖细胞是如何移动的,以及它们的移动是否与它们的最终命运相关,来进一步研究这个问题。”通过记录早期胰腺中荧光标记的单个祖细胞的三维电影,我们意识到祖细胞在它们的命运决定之前,会继续改变它们的位置来塑造胰腺的结构,”该研究的第一作者DanStem助理教授Pia Nyeng解释说。哥本哈根大学。
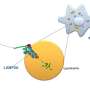
该观察强烈表明细胞的束缚似乎不会被预先确定,而是由最终目的地的特定利基确定。为了检查如何控制器官中细胞的最终定位的最终定位,研究人员发现信号蛋白P120CTN发挥着重要作用。
“该蛋白质影响细胞之间的粘附性(粘性)。与具有P120CTN表达低表达的细胞相比,具有高表达P120CTN的细胞更加粘合。我们观察到具有高表达P120CTN的细胞留在胰腺的中心部分中,而细胞对于低表达P120CTN迁移到胰腺的周边部分。为了测试我们的理论,我们通过杀死编码P120CTN的基因来降低血管中央部分内的少数祖细胞中的粘附性。通过使用电影分析这些细胞的行为我们看到他们迁移到胰腺的外周部分,并开发成酶产生的缩醛细胞。“
可能会减慢转移
癌症的扩散强烈地连接到癌细胞的粘合性能下降。减少粘合使器官中的癌细胞使得它们来自的利基,并侵入包括血管的周围组织,以将其转移到其他器官。因此,癌症研究专注于试图防止粘附的降低,或者在癌细胞中恢复高粘附性,而不令人担忧这是否可能导致较高的粘附性比健康细胞更高。
“我们的实验表明,促使细胞分离的是它们在粘附方面的内在差异。这表明,决定癌细胞是否分离(在癌症中侵袭邻近组织)的不是细胞本身的粘附特性,而是细胞与邻近细胞的相对粘附。因此,为了抵消转移,癌症治疗应尽量恢复正常水平粘附。“
“P120CTN介导的器官图案化之前并确定了胰腺祖先命运”已发表在细胞发育。
进一步探索













用户评论