科学家如何研制出治疗多发性硬化症的突破性药物

想象一下,一觉醒来,眼前的世界一片模糊。去厨房吃早餐时,你感到一阵疲惫,胳膊和腿都像铅一样。这就是40多万多发性硬化症患者的现实,多发性硬化症是美国最常见的神经系统疾病之一。MS会导致进行性神经和大脑损伤,因为身体会攻击每个神经细胞周围的保护层(称为髓鞘)。它会导致视力下降、腿部无力和麻木,最终导致残疾。有两种类型:复发缓解型和原发性进展型。在复发缓解型MS(更常见的形式)中,患者经历症状发作,随后是恢复期。在原发性进展性多发性硬化症中,没有复发期,患者病情稳步下降。
尽管这种情况的记录可以追溯到几百年前,但直到最近25年,第一批具有适度疗效的药物才被批准用于治疗多发性硬化症。然而,直到去年,还没有一个真正有效的方法来控制它。2017年,美国食品和药物管理局(FDA)批准了ocrelizumab,这是一种已被证明可以显著减缓疾病进展的药物,也是首个被批准用于治疗原发性进展性多发性硬化症的药物。它被誉为一种突破性药物。
但是为什么这种药没有早点出现呢?
与普遍的看法相反,大多数药物的发现都不是灵光一现的产物!这是世界各地的科学家和医生数十年研究、试错和坚持不懈的结果,每个人都从别人的发现和错误中学习。
“药物发现可以是随机行走,”耶鲁医学院神经病学主席大卫·a·哈夫勒医学博士说。“研究人员可以选择做无数的实验。最终找到治愈方法的方法很大程度上取决于运气。”
哈夫勒博士应该知道:他发表了402篇论文,是被引用最广泛的在世神经学家之一,对复杂的医学有数十年的第一手经验。他还在识别潜在的生物过程方面发挥了重要作用多发性硬化症.“Ocrelizumab是治疗多发性硬化症的一个重要里程碑,”Hafler博士说。“这种药物令人兴奋的地方在于,它让我们深入了解其原因。”
以下是它是如何形成的。
多发性硬化症是一种神秘的疾病
1868年,被称为“现代神经学之父”的让-玛丽·夏科特(Jean-Marie Charcot)解剖了一位患有(我们现在认为的)多发性硬化症的已故患者的大脑,发现了遍布脊髓、脑干和大脑白质的硬化斑块,这表明神经受损。从那时起,科学界开始怀疑这种疾病是一种影响神经系统的疾病。这种疾病因其一系列症状而没有明显的根本原因而困扰着医生。“这也是第一次有人把多发性硬化症确定为一种独特的疾病,”哈夫勒博士说,他的办公室里有一尊夏科特博士的半身像。
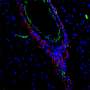
后来,当新的显微镜技术允许科学家进行观察时,夏科特博士的发现得到了证实神经细胞更详细地说。20世纪初,爱丁堡大学的科学家詹姆斯·道森(James Dawson)利用这项技术观察了多发性硬化症患者血管周围的炎症和髓磷脂(保护神经细胞的脂肪覆盖物)的损伤。这种损伤不同于医生以前见过的任何损伤。那么,是什么引起的呢?
由于道森博士(以及后来的研究人员)描述了血管周围的炎症,一些科学家认为多发性硬化症是由血液循环中的一种毒素泄漏到大脑引起的。其他人则能够通过阻断实验室动物大脑的血液流动来模拟髓磷脂的损伤,指出循环问题是潜在的原因。还有人认为MS可能是由病毒引起的。
因此,有不同的理论,但一个很有前途的理论出现在1933年,纽约市洛克菲勒研究所的托马斯·里弗斯给恒河猴注射了无病毒的髓磷脂,令人惊讶的是,这导致免疫系统攻击自己的身体。这些猴子随后表现出与多发性硬化症患者相似的症状。这个现在被称为实验性自身免疫性脑脊髓炎(EAE)的模型被认为是一个突破——它允许科学家们更仔细地观察一个与多发性硬化症患者表现出相同类型神经损伤的活体体内发生了什么。
该模型还表明,多发性硬化症不是由病毒引起的。但就像病毒反应一样,这种疾病似乎仍然涉及免疫系统。1960年,神经免疫学家菲利普·帕特森(Philip Paterson)在一个现在看来“经典”的实验中,通过向EAE小鼠注射淋巴细胞(一种参与脑神经系统疾病的白细胞),能够将ms样症状转移到健康大鼠身上免疫反应)。他选择淋巴细胞是因为淋巴细胞存在于已故多发性硬化症患者的脑斑块中。
哈夫勒博士说:“在这一点上,试图证明多发性硬化症的其他假说都陷入了死胡同,而免疫系统理论似乎有了脚。”“所以,这就是我们决定追求的目标。”
MS会使身体与自己对抗
免疫系统引起了哈夫勒博士的兴趣——甚至在他还是个孩子的时候。10岁时,他开始看着自己的红色和白细胞(在用大头针扎自己之后)在玩具显微镜下。六年级时,他知道自己想成为一名免疫学家。后来,他师从几位研究多发性硬化症的世界知名科学家,包括戴尔·麦克法林、亨利·昆克尔和霍华德·韦纳。
从医学院毕业后,哈夫勒博士想要解决围绕多发性硬化症尚未解决的问题。“我对大脑和免疫系统很感兴趣,这两者自然而然地结合在了一起,”他说。
到目前为止,使用EAE模型的研究已经表明T细胞(一种白细胞,是免疫反应的一部分)和多发性硬化症之间存在联系。哈夫勒博士想更好地了解这些细胞。在20世纪90年代,他的实验室率先重建了能够攻击髓磷脂蛋白的T细胞,并在2002年在人体中发现了一种特殊类型的T细胞,它可以在免疫系统完成任务后抑制或镇定免疫系统。这些细胞被称为调节性T细胞,可以防止身体在自身免疫反应中攻击自己的细胞。在多发性硬化症患者中存在缺陷。
遗传因素
大约在同一时间,研究开始显示患有多发性硬化症的双胞胎有相关的患病风险。但这很复杂:研究表明,MS发生在兄弟姐妹和异卵双胞胎中的比例很小,但在同卵双胞胎中约有25%。这意味着遗传与多发性硬化症有关,但这不是唯一的原因。
哈夫勒博士对这种基因成分很感兴趣。他说:“我对免疫学感到沮丧——有太多移动的部件,很难知道该研究免疫系统的哪个部分。”但在遗传学方面,有一条明确的前进道路。
哈夫勒博士帮助成立了国际多发性硬化症遗传学联盟(International Multiple Sclerosis Genetics consortium),该联盟汇集了来自18个国家30个机构的研究人员。通过结合多项研究的数据,该联盟收集了数千名多发性硬化症患者的基因组数据,并将其与数千名没有这种疾病的人进行了比较。结果,他们能够识别出233种基因变异,这些基因结合在一起会增加一个人患多发性硬化症的几率。
偶然的发现
科学家们用来研究多发性硬化症的动物模型仍然没有完全模拟这种情况。这是斯蒂芬·豪瑟在20世纪90年代初在实验室工作时的想法。这位科学家想起了他的导师在麻省总医院完成神经病学住院医师实习时告诉他的一些事情:EAE模型和多发性硬化症的病理是不同的——具有MS样症状的小鼠的组织变化与人类MS不完全吻合。
也许他的同事们还没能弄清楚多发性硬化症的原因是因为他们一直在一个不准确的模型上进行实验。
豪泽博士花了数年时间对各种模型进行实验,1995年,他的研究团队终于能够诱导出与人类MS完全相同的MS。但还有更多的东西:T细胞的转移不会像在EAE模型中那样引起MS。只有在他们同时转移T细胞和b细胞抗体后,他们才能够诱导多发性硬化症。
这是一个意外。几十年来,科学家们只关注T细胞。那么,B细胞——免疫系统中的另一种细胞,也是免疫反应的一部分——是如何与这种情况相吻合的呢?
豪泽博士的假设是,B细胞以某种方式触发T细胞引起MS攻击。他想尝试针对B细胞的药物测试。巧合的是,一种名为利妥昔单抗(rituximab)的新药刚刚被FDA批准用于治疗一种名为非霍奇金淋巴瘤的自身免疫性疾病。这是第一个被批准的针对B细胞的治疗方法。
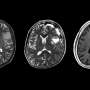
豪泽博士的团队在2008年发表了一项开创性的研究。该研究跟踪了104例MS患者,其中69例已接受利妥昔单抗治疗。与安慰剂组相比,利妥昔单抗组新脑损伤的形成(多发性硬化症患者髓鞘攻击的常见标志)减少了91%。这项研究表明,B细胞不仅以某种方式在引起疾病中发挥了作用,而且当B细胞被药物消耗殆尽时,大脑炎症几乎立即被关闭。
六年后,经过多次临床试验,FDA批准了一种模仿利妥昔单抗的药物。这种药物是ocrelizumab。
虽然还不清楚这种药物是如何起作用的,但科学家们知道它可以删除循环中的B细胞,从而防止攻击髓磷脂的异常T细胞免疫反应。
Ocrelizumab是首个被批准用于原发性进展性MS的药物,这是该疾病最具侵略性的形式,在这种疾病中,大脑和身体会稳步恶化。临床试验表明,服用ocrelizumab剂量的患者在24周后脑部病变明显减少,复发缓解型MS(最常见的MS类型)患者的复发率较低。这种药物击败了干扰素- 1a,后者是治疗多发性硬化症最常用的药物之一,在降低每年复发率和MRI扫描发现的病变数量方面。
理解多发性硬化症是一个持续的过程
所以,有一些答案。但更多的问题仍然存在。B细胞对T细胞做了什么来触发MS?基因在这一切中扮演了什么角色呢?
这些都是哈夫勒博士的实验室正在努力解决的问题。目前,他们正在使用一种叫做单细胞RNA测序的新技术来观察MS患者治疗前后受影响的细胞类型,以更好地了解这种疾病背后的基本生物学。他的研究也代表了对常规科学研究方式的背离。
哈夫勒博士说:“虽然大多数科学都是建立模型,但我们决定先观察,然后根据观察得出假设。”
此外,之前的研究表明,盐和脂肪可能会导致调节性T细胞功能障碍,这表明环境因素可能是一个难题。哈夫勒博士的实验室正在继续调查这些因素究竟是如何影响患者患多发性硬化症的风险的。
Ocrelizumab本身也不是治疗之路的终点,目前还没有关于其长期副作用的研究。从好的方面来看,它的临床试验结果优于市场上所有其他MS药物,并将MS复发患者的年复发率降低了50%。然而,它只能为患有原发性进展性疾病的患者提供大约25%的益处。这使得研究人员想知道是否有不同的生物机制在起作用。
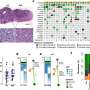
不过,哈夫勒博士仍然抱有希望。2014年,他的实验室在《自然》杂志上发表了一篇论文,绘制了不同条件下细胞的基因图谱。他们发现,在多发性硬化症的遗传过程中,参与最多的细胞是免疫细胞,而不是脑细胞,这进一步证实了多发性硬化症是一种自身免疫性疾病,而不是神经系统疾病。
哈夫勒博士说:“这是一条漫长而曲折的道路。”“在我们找到所有答案之前,这种情况可能会继续下去。但我们有最好的科学家在研究,我有信心它会成功的。”