髓鞘的形成是由蛋白质分子调节的
据德国多发性硬化症协会(German Multiple sklererose Gesellschaft)称,德国约有20万人患有多发性硬化症(MS),这是一种严重的神经系统疾病,目前尚无治愈方法。虽然原因未知,但研究人员知道免疫系统错误地攻击了神经纤维周围的保护鞘。由Michael Wegner教授领导的一个科学家团队在Friedrich-Alexander-Universität Erlangen-Nürnberg (FAU)与来自德国Münster的研究人员合作,现在已经发现了髓鞘的形成是如何受到蛋白质分子的调控的。这一发现可用于刺激复发后新髓鞘的形成。
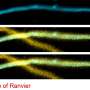
人类的大脑被比作一台高性能的计算机,在这台计算机中,众多独立的处理器必须尽可能有效地通过高速电缆连接在一起。在900到1000亿个神经细胞中,每一个都代表处理器,以及被覆盖的神经纤维或轴突髓鞘代表光纤电缆。传输信息的速度高度依赖于质量髓鞘护套,由特殊的脑细胞形成,称为oligodendrocytes。对髓鞘的损伤或产生它们的细胞导致严重的疾病,例如MS。这种疾病最终导致神经细胞被破坏。
髓磷脂的形成有复杂的机制
由FAU生物化学和病理生物化学主席Michael Wegner教授领导的工作组正在研究少突胶质细胞如何调节髓鞘的形成。像多发性硬化症这样的神经系统疾病只能用这种知识来理解。工作组已经确定蛋白质像Sox10这样调节髓鞘形成和保存的分子。
新项目的目的是了解所识别的蛋白质在形成髓鞘时如何相互作用。研究人员发现,在已知分子之间的这种相互作用是成功的,需要称为NFAT蛋白的其他分子。这些主要以其在免疫系统中的功能而闻名。在少突胶质细胞中存在NFAT蛋白的存在确保所有其他所需的蛋白质分子可以在这些细胞中一起存在而不会彼此移位。
在他们的研究中,最近发表在自然通讯,由Matthias Weider博士和Tanja Kuhlmann博士从UniversitätsklinikumMünster的团队领导的Wegner的工作组教授展示了所涉及的精确生物化学机制。NFAT蛋白的抑制对大鼠,小鼠和人类的寡替蒙胶质细胞的能力产生不利影响,以形成髓鞘。实际上,这些蛋白质在受MS的脑部的部分脑中的寡替蒙胶质细胞中。但是,尚不清楚这是否是损坏的原因之一。“相互关系非常复杂,”迈克尔威纳说。
调查结果不仅与基础研究有关,也不是医学。未来可能使用针对NFAT蛋白的刺激,以促进MS患者的新髓鞘鞘,例如在复发之后。但是,这种刺激物质尚未使用。到目前为止,仅开发了抑制NFAT蛋白活性的物质,例如环孢菌素A和Tacrolimus。它们用于医药,主要用于使免疫系统进行控制,从而防止器官排斥在移植患者中。一个有趣的事实是,这些患者经常患有由髓鞘损失引起的神经系统疾病。新的研究表明,这些严重的副作用是药物抑制NFAT蛋白的直接结果。因此,这种药物改善了这一点非常重要。
这一发现证明了Nfat蛋白对髓磷脂形成的重要意义,并为目前无法治愈的神经疾病的治疗开辟了新途径。
进一步探索









用户评论