青光眼基因治疗进展

在测试通过降低眼内压力来治疗青光眼的基因时,威斯康星大学麦迪逊分校的科学家们偶然发现了一个问题:他们无法有效地将基因传递到控制眼内液体压力的细胞中。
基因只有进入细胞才能发挥作用。
青光眼是最常见的致盲疾病之一,由眼内压力过大引起,通常是由于液体排泄堵塞。威斯康星大学麦迪逊分校的眼科学和视觉科学教授保罗·考夫曼说:“大多数青光眼可以通过日常药物治疗来治疗。”“替换基因从理论上讲,它可以连续多年恢复正常的液体流动,而不需要每天自己服用眼药水,这很不方便,可能会产生局部甚至全身的副作用。”
在今天发表在科学杂志上的一项研究中调查眼科学和视觉科学考夫曼和威斯康星大学麦迪逊分校眼科学和视觉科学教授柯蒂斯·勃兰特(Curtis Brandt)展示了一种将新基因输送到引流管的改进策略,这种策略被称为小梁网。
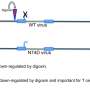
同事们一直在测试一种基于猫免疫缺陷病毒(FIV)的载体来传递基因。比如相关的人类免疫缺陷病毒在美国,FIV可以将基因插入宿主的DNA中。然而,眼睛对FIV的先天防御干扰了分娩。
病毒颗粒包含基因包裹在蛋白质外壳和脂质膜中。在病毒进入细胞并脱膜后,来自宿主的防御性分子可以“将病毒颗粒拖到细胞的垃圾处理场,即蛋白酶体,在那里被降解,”Brandt说。“我们想知道暂时阻断蛋白酶体是否可以防止基因传递载体的破坏并增强传递。”
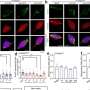
在目前的研究中,携带标记蛋白的FIV病毒被放置在小梁网的细胞上,使用或不使用阻止蛋白酶体的化学物质。
勃兰特说,在超过剂量阈值的情况下,进入靶细胞的基因转移大约增加了一倍。新的基因也在网状组织中更加均匀地分布。传递更多的基因副本应该会产生更大的治疗效果,打开网状引流,降低眼内压力。
勃兰特说,目前的研究关注的是转移基因的工具,而不是基因本身。但他说,即使在目前的研究之前,他和考夫曼“已经确定了至少两个可以堵塞排泄的基因”。
在替换基因和治疗疾病的长期斗争中,“眼睛一直是最大的成功故事之一,”勃兰特说。一种叫莱伯氏先天性黑蒙的致盲眼病会损害保持光敏的细胞功能细胞健康;替换突变基因可以保护甚至改善年轻患者的视力。这种基因疗法目前正在等待食品和药物管理局的批准。
为了预防注射病毒带来的危险,“我们取出了几乎所有的病毒病毒’基因,所以它没有机会从最初注射的地方复制和传播,”勃兰特说。
虽然这项技术确实会干扰眼睛中的抗病毒防御,但效果是暂时的。勃兰特说:“你遇到这种药物一次,它就会被代谢掉,固有的抑制作用就消失了。”
“我们已经证明,这种策略在眼器官培养中确实有效,”勃兰特说。“一旦我们进一步提高效率,确定要传递哪种基因,那么我们可能就准备好进行临床试验了。”