帕金森病背后的批判性有毒物种是第一次在工作中瞥见
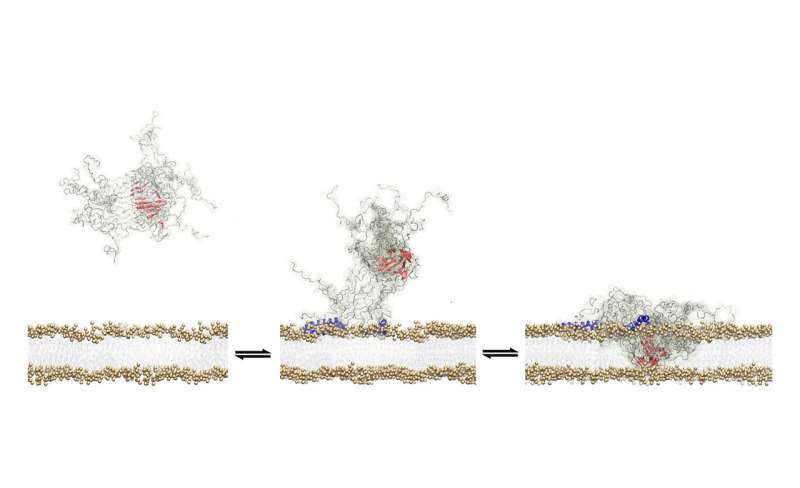
研究人员已经瞥见了与帕金森病有毒的蛋白质簇如何破坏健康脑细胞的膜,产生细胞壁中的缺陷,最终导致一系列诱导神经病死亡的事件。
研究检测了所谓的有毒低聚物,当个体蛋白质混浊并聚集在一起时出现的蛋白质分子簇。在帕金森病的情况下,所涉及的蛋白质被称为α-核蛋白当它正常运作时,它在大脑信号传递中起着重要的作用。
这些聚集的形成和传播被认为是这种进展性疾病的潜在分子机制的关键组成部分。了解它们是如何进入和破坏细胞的,为开发新的和更有效的治疗方法提供了机会。但到目前为止,研究它们如何损害脑细胞一直是极其困难的,因为它们通常是不稳定的。形成后不久,它们要么分解,要么组装成对单个细胞伤害较小的更大的结构。
在这项新的研究中,学者们能够在足够长的时间内稳定低聚物,以前所未有的细节检查它们是如何破坏脑细胞壁的。他们发现了这种低聚物的一个特殊特征,它可以吸附在细胞壁,和一个“结构核心”,然后断裂。
这项研究是由来自英国、意大利和西班牙的科学家组成的国际团队进行的,该团队由剑桥大学的克里斯托弗·多布森教授和伦敦帝国理工学院的阿方索·德·西蒙博士领导。
德西蒙解释说:“低聚物的一个共同特性是,一旦它们与表面结合,就会损害脑细胞。”“这有点像把一块非常热的金属放在塑料表面上。在相当短的时间内,它会在塑料上烧出一个洞。当低聚物接触到细胞膜时,它会做类似的事情,这会破坏细胞膜的完整性,而这是导致神经元死亡的机制中的关键步骤。”
剑桥大学圣约翰学院的博士后研究员朱利亚娜·弗斯科博士在攻读博士学位期间完成了该研究的大部分实验工作,她说:“仅仅拥有这些信息并不意味着我们现在就可以去制造一种药物,但显然,如果我们能理解这些蛋白质团块的行为方式,我们就可以在治疗帕金森病方面取得更快的科学进展。”这意味着我们可以采取更理性的方法来发现药物。”
有毒的低聚物形成于导致帕金森病的一系列事件的早期阶段,据信,这始于阿尔法突触核蛋白发生故障并开始粘在一起。在这种情况下,它们的出现对神经元功能是致命的。一旦低聚物形成,它们就会分散,并使最初的毒性扩散到其他细胞。
在该研究中,研究人员使用固态核磁共振光谱(SSNMR)检查了毒性和无毒形式的毒性和无毒形式的实验室样品。该技术的最新进展使他们能够在以前不能进行的细节水平中研究低聚物。该研究团队表征了结构的不同特征,然后研究了这些各种性质的影响如何影响它们与样本的相互作用大脑细胞取自老鼠,以及额外的细胞取自人脑肿瘤。
这项研究的结果尤其可以帮助我们识别能够攻击这些有害毒素的分子,从而限制它们的影响。今年10月,剑桥大学在化学系成立了一个新的错误折叠疾病中心,旨在开发包括帕金森病在内的一系列疾病的治疗策略。它的大部分工作将建立在研究的基础上,比如这个研究,加强了对神经退化的基本过程的科学理解。由此,可以确定未来可能用于药物的分子“候选”,并在必要时进行优化,以靶向疾病。
Dobson教授,谁是圣约翰大学,剑桥,剑桥和误折叠疾病中心的董事,说:“关于这项工作的真正令人兴奋的事情之一是,这不仅有可能定义结构的结构神经退行性疾病中的批判性致病性物种,但我们也设法提出了一种毒性的机制,为追求理性治疗策略提供重要的线索......“
这篇题为a-synuclein寡聚物引起细胞膜破裂和细胞毒性的结构基础的报告发表在该杂志上科学。










用户评论