团队测试潜在艾滋病毒疫苗的最佳交付方式
几十年来,艾滋病毒已经成功地躲过了研制有效疫苗的所有努力,但斯克里普斯研究所(TSRI)和拉霍亚过敏与免疫学研究所(LJI)的研究人员正在稳步接近这一目标。他们的最新研究发表在最新一期的免疫力的研究表明,优化疫苗注射方式和时间对于在临床前模型中诱导保护性免疫反应至关重要。
与其他因素相比,皮下注射候选疫苗和增加免疫间隔时间更能提高免疫效果实验性疫苗并可靠地诱导中和抗体。中和抗体是有效的关键成分免疫反应.在它们能在体内站稳脚跟之前,它们就会抓住入侵病毒并使其失去活性。众所周知,它们很难被HIV病毒产生。
TSRI教授Dennis R. Burton博士同时也是国际艾滋病疫苗倡议(IAVI)中和抗体中心和国家卫生研究院艾滋病毒/艾滋病疫苗免疫学和免疫原发现中心(CHAVI-ID)的科学主任,他说:“这项研究是通向艾滋病疫苗的漫长旅程中的一个重要阶段。”“候选疫苗我们在这里合作的可能是最有前途的原型,其中一个将在2018年进入人体,”伯顿说。
LJI疫苗发现部门的教授、资深合著者Shane Crotty博士补充说:“之前有很多大的问号,而这项研究的目的是在我们进入人体临床试验之前得到尽可能多的答案。”“我们有信心,我们的研究结果将具有预测性。”
艾滋病毒已经从头条新闻中消失,主要是因为抗逆转录病毒药物的发展已经把艾滋病变成了一种可控制的慢性疾病。然而,目前全球约3670万艾滋病毒感染者中,只有大约一半能够获得控制病毒所需的药物。与此同时,新感染率仍然居高不下,这强调了采取措施的必要性预防性疫苗.
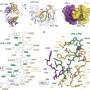
这些最新的发现是十几个研究团队多年来通力合作和艰苦研究的结果,他们围绕着人造蛋白质三聚体的开发、改进和研究,这些蛋白质三聚体逼真地模拟了在病毒表面发现的蛋白质峰值。这项工作的核心是由TSRI自己的William R. Schief博士、Andrew B. Ward博士、Ian A. Wilson、D.Phil组成的CHAVI-ID免疫原工作组。理查德·t·怀亚特博士,以及克罗蒂和伯顿。这组实验室与麻省理工学院教授Darrell J. Irvine博士和阿姆斯特丹大学教授Rogier W. Sanders博士合作,提供了研究中测试的前沿免疫原。
重组三聚体,或称为sosip,在早期的小型研究中是不可靠的非人灵长类动物.非人灵长类动物,特别是恒河猴,被认为是HIV疫苗研究最合适的临床前模型,因为它们的免疫系统与人类的最相似。
“这些动物的免疫反应,虽然是正确的那种,但不是很强大,有一些根本没有反应,”科林·哈维纳尔-多尔顿博士解释说,他是克罗蒂实验室的科学助理。“这引起了人们的极大担忧,在人类临床试验中,这种免疫原不会持续在所有个体中引发有效的免疫反应。”
为了可靠地诱导中和性抗体反应,合作者同时测试了三聚体和免疫方案的多种变体,以确定下一步的最佳策略。Crotty、Burton和他们的同事与dr . Dan baruch教授合作,他是Beth Israel女执事医疗中心病毒学和疫苗研究中心主任,负责协调免疫接种。
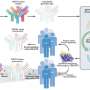
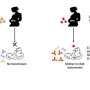
这项研究的设计在很大程度上是根据合作者在之前的一项研究中所了解到的,通过对淋巴结的精细针刺取样,科学家观察到滤泡辅助T细胞有助于指导产生抗体的B细胞的成熟步骤。皮下注射疫苗而不是更传统的肌肉注射方式,间隔在8周而不是更常见的4-6周注射疫苗,可靠地在所有动物中诱导了强烈的功能性免疫反应。
使用渗透泵在两周内缓慢释放疫苗,在非人灵长类动物中进行SOSIP免疫后,产生了有史以来最高的中和抗体滴度。虽然渗透泵不是一种实用的疫苗输送方式,但它们说明了一个重要的问题。“这取决于我们如何给予疫苗伯顿实验室的研究生、该研究的联合第一作者马蒂亚斯·波特纳(Matthias Pauthner)说,由于免疫途径的不同,两者之间的差异比我们预测的要大。“我们可以帮助把我们现在知道的转化为临床。”
进一步探索