心脏干细胞疗法的设计灵感来自于身体本身
在心脏病发作期间,临床上称为急性心肌梗死(MI),心肌细胞严重受损并最终死亡。
根据美国心脏协会的数据,心肌梗死是全球死亡的主要原因。这在一定程度上是由于人类心脏修复或再生其细胞(即心肌细胞)的能力有限。在过去的十年中,干细胞疗法已被探索作为一种再生心肌细胞的方法,但结果好坏参半。
俄亥俄州立大学的研究人员在生物医学工程教授何晓明的带领下,发明了一种新的干细胞治疗方法,这种方法受到大自然的启发,前景广阔。研究结果发表在本期的《科学》杂志上自然通讯他们的方法显著提高了植入的存活率干细胞与传统方法相比。
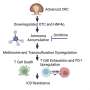
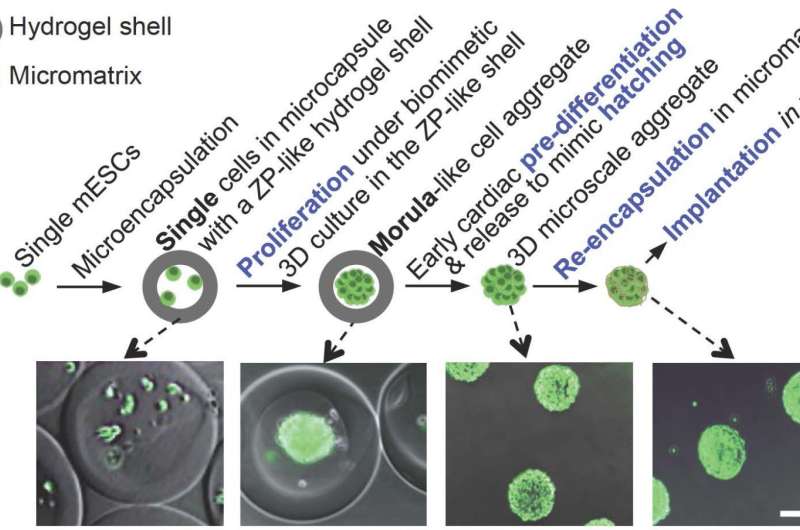
研究人员的准备多能干细胞因为植入心脏类似于女性身体在生殖过程中准备胚胎细胞植入子宫壁,即预分化和包封两个阶段。多能干细胞几乎可以制造出人体自我修复所需的任何细胞或组织。
自然繁殖的步骤包括细胞有组织的增殖,形成一个聚集体,或桑葚胚,包裹在一个薄的保护水凝胶壳。同样地,研究人员将老鼠封装起来胚胎干细胞在一个半透水凝胶壳包裹的小核里,它们在那里增殖。这种类似胚胎的结构极大地帮助保留了贺建奎所说的干性,即细胞在没有自发分化的情况下自我更新的能力。女性生殖系统的下一步是将桑葚胚预先分化为更特定的细胞类型。在心肌梗死治疗研究中,研究人员将聚集的干细胞预先分化为早期心脏阶段。
贺建奎说,将细胞预分化到早期心脏阶段是至关重要的,因为它似乎可以最大限度地减少当前再生医学方法中的一个常见问题——畸胎瘤的形成,畸胎瘤可以发展成良性或恶性肿瘤。
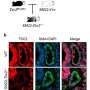
“这些细胞致力于成为心肌细胞,”他说,“但还没有完全实现。”这个精确的时间是由细胞生物标记物决定的。微阵列和流式细胞仪数据分析表明,聚集的细胞在预分化后成功地定向到早期心脏系。
在自然界中,人类胚胎细胞在预先分化的胚泡中,胚泡会短暂地从果冻状的外壳中孵化出来,然后在植入子宫壁之前被重新包裹在一个称为滋养层的新壳中。研究人员模拟了这些步骤,释放聚集的早期心脏细胞,并将它们重新包裹在生物相容性和可生物降解的支架中,然后植入受损的小鼠心脏。
他解释说:“这种微基质再封装过程与传统的支架工程相反,传统的支架工程首先制造支架,然后在支架上播种细胞。”
重新封装对于暂时将植入细胞与宿主免疫系统隔离也是至关重要的,这样细胞就可以适应宿主微环境而不引起明显的免疫反应。这保证了细胞的高存活率。在临时微基质中重新封装后,贺建奎和他的同事们将细胞聚集物注射到近期出现心脏病发作损伤的小鼠体内。
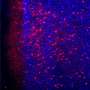
植入的细胞在人体心脏诱导的化学、机械和电子信号的引导下,显示出再生心脏组织的出色能力。注射包膜多能干细胞可显著减少心肌梗死小鼠的纤维化,恢复心肌功能,提高动物存活率。
他说:“我们的生物启发方法是基于模仿自然现象,在制备多能干细胞治疗心肌梗死和其他潜在缺血性疾病方面具有多重优势。”
他说,下一步是进行人类心脏再生的研究,届时研究人员将开始使用从人类皮肤、脂肪或其他组织中提取的诱导多能干细胞。
项目合作者包括生物医学工程教授张明军、韦克斯纳医学中心病理学家、副教授沈如龙、韦克斯纳医学中心医师、医学院教授刘振国、医学院副教授Noah Weisleder,以及来自生物医学工程和戴维斯心肺研究所的研究生和博士后研究员。
他说:“这项研究是工程学、细胞生物学、生理学、病理学和临床医学专业知识完美结合的结果。”“在俄亥俄州立大学,所有这些专家都位于附近。”
这项研究得到了美国国家科学基金会和国立卫生研究院的部分资助。