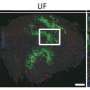
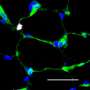
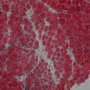
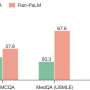
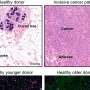
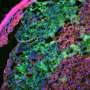
基因控制受伤的肌肉成体干细胞的再生
一个关键基因使修复受伤的肌肉在整个生命。这是老鼠的一项研究发现由纽约大学Langone医学中心的研究人员和科罗拉多大学博尔德分校,和7月21日在网上发表细胞的报道。
研究结果进一步表明,这个“被忽视的”基因可能在sarcopenia扮演着重要的角色,随着年龄的增长肌肉组织的损失。
具体地说,该研究小组发现,单个蛋白质水平称为AUF1确定池干细胞保持肌肉损伤后再生的能力,老鼠的年龄。动作的变化AUF1也与过去的研究人类肌肉疾病。
30多基因疾病,统称为肌肉疾病,这个再生过程中功能缺陷,导致肌肉削弱或浪费。临床表现和诊断年龄各不相同;杜氏肌萎缩症多发生于婴儿,肢带肌萎缩症削弱了躯干和四肢的肌肉开始在成年早期,和sarcopenia发生在老年患者。
“这工作场所内的某些肌肉疾病直接的起源肌肉干细胞,表明AUF1控制器是一个至关重要的成人肌肉干细胞的命运,”罗伯特•施奈德博士说,阿尔伯特·b·萨宾教授微生物学和分子发病机制和治疗联盟办公室副主任在纽约大学兰贡。
“干细胞供应非常贫AUF1信号是有缺陷的,让肌肉更加恶化每次受伤后修复失败,”施奈德说。
毁灭的标记
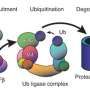
研究结果围绕基因表达的一部分,指令编码的DNA链的蛋白质是由中间体建设称为信使rna (mrna)。蛋白质组成人体的结构,酶和信号。某些基因的表达需要快速开启和关闭控制部分的目标破坏mRNA中间体,工作分配给像AUF1蛋白质。
函数之间的调查人员发现,信使rna控制的稳定是干细胞的命运,它来自人类胚胎,然后用专门在子宫里,直到他们成为我们的骨骼,皮肤、肌肉和其他组织类型。一些组织保持专业的干细胞池到成年,准备成熟的替代细胞和再生受损组织。
骨骼肌损伤后,肌肉干细胞接收信号相乘,修复受损组织,研究者发现这一过程由AUF1控制。AUF1的mRNA目标中肌肉干细胞,他们发现一个编码一个成人肌肉再生的“支配性调控因子”,一种称为MMP9的蛋白质。这种酶分解其他蛋白质,最终控制他们的表达水平。
目前的研究发现,缺乏AUF1基因小鼠显示MMP9活动增加和减少stem-cell-driven修复。这种“自我破坏”干细胞池通常修复肌肉和摧毁他们的肌肉干细胞的利基居住,因为他们等待激活。在一起,这导致了一个戏剧性的和持续的骨骼肌。
研究人员表明,他们可以恢复正常的肌肉干细胞及相关函数肌肉在小鼠缺乏AUF1再生再利用的癌症治疗药物开发区块MMP9的活动。
“这提供了一个潜在的临床治疗路径,加速肌肉再生创伤性损伤后,或在某些类型的成人患者出现肌肉萎缩症,”施奈德说。“我们可以治疗各种退行性疾病增强居民组织干细胞通过针对MMP9及其途径,甚至那些与正常AUF1。”
”,曾一度被认为AUF1没有超过标记mrna,是不需要,所以他们可以处理的,功利的蛋白质的小利益,”第一作者德文郡Chenette说,毕业学生率先在施耐德的实验室工作。“相反,我们的结果表明,AUF1已经演变成为一个干细胞命运调控的重要和相关的再生能力的成年组织。”